��Ŀ����
����Ŀ���±���Ԫ�����ڱ���һ���֣�����Ա������б��Ϊ�١����Ԫ�ػش��������⡣
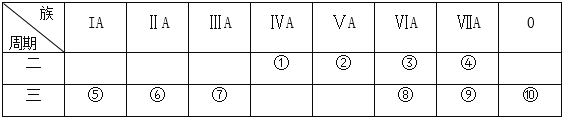
��1���ǽ�������ǿ��Ԫ����______(��Ԫ�ط��ţ���ͬ)���γɻ�������������Ԫ����_____������õ�Ԫ����___________��
��2����������Ԫ�س�����ԭ�Ӱ뾶��С����______(��Ԫ�ط���)����ЩԪ�ص�����������Ӧˮ�����м�����ǿ����__________(�ѧʽ����ͬ)���������Ե���____________������������Ӧˮ������������ǿ����__________��
��3���ޢߢ��γɵļ����ӵ���С�����˳���� ______________�������ӷ��Żش����⣩��
������Ӧ���⻯��Ƚ��ȶ�����_________���ѧʽ����
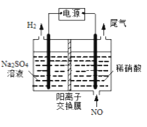
��4���ݺ͢ۿ����γ����ֻ�������п�����������߹����������ʵĵ���ʽΪ_________��������ѧ��������Ϊ _______________��
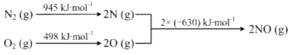
��5��������γɵĻ�����Ľṹʽ __________���õ���ʽ��ʾ ��������γɻ�������γɹ��� _________________________��
���𰸡� F C Ar Cl NaOH Al(OH)3 HClO4 Al3+<Mg2+<Cl- HCl ![]() ���Ӽ����Ǽ��Լ�
���Ӽ����Ǽ��Լ� ![]()
![]()
������������Ԫ�������ڱ��е�λ��֪���١����Ԫ�طֱ���C��N��O��F��Na��Mg��Al��S��Cl��ArԪ�ء�
(1)�ǽ�������ǿ��Ԫ��λ�����ڱ����Ͻǣ���ϡ��������⣬ΪFԪ�أ��γɻ�������������Ԫ����CԪ�أ�����õ�Ԫ���Ƕ���Ԫ�أ�ΪAr���ʴ�Ϊ��F��C��Ar��
(2)ͬһ����Ԫ�أ�ԭ�Ӱ뾶����ԭ�������������С�����Ե�������ԭ�Ӱ뾶��С��Ԫ����ClԪ��(ϡ���������)��Ԫ�صĽ�����Խǿ��������������ˮ�������Խǿ�����Ե������ڼ�����ǿ����NaOH�������Ե�����������������������ѧʽΪAl(OH)3��Ԫ�صķǽ�����Խǿ��������������ˮ��������Խǿ������������Ӧˮ������������ǿ����HClO4���ʴ�Ϊ��Cl��NaOH��Al(OH)3��HClO4��
(3)һ����ԣ����ӵĵ��Ӳ���Խ�࣬���Ӱ뾶Խ���Ӳ�����ͬʱ���˵����Խ�����Ӱ뾶ԽС���ޢߢ��γɵļ����ӵ���С�����˳��ΪAl3+<Mg2+<Cl-��Ԫ�صķǽ�����Խǿ���⻯��Խ�ȶ���������Ӧ���⻯��Ƚ��ȶ�����HCl���ʴ�Ϊ��Al3+<Mg2+<Cl-��HCl��
(4)�ݺ͢ۿ����γ����ֻ�����Ϊ�����ƺ������ƣ����п�����������߹�����������Ϊ�������ƣ�����ʽΪ![]() ��������ѧ��������Ϊ���Ӽ����Ǽ��Լ����ʴ�Ϊ��
��������ѧ��������Ϊ���Ӽ����Ǽ��Լ����ʴ�Ϊ��![]() �����Ӽ����Ǽ��Լ���
�����Ӽ����Ǽ��Լ���
(5)CS2�Ľṹ�������̼���ƣ��ṹʽΪ![]() ���Ȼ�þ�������ӻ�����õ���ʽ��ʾ�Ȼ�þ���γɹ���Ϊ
���Ȼ�þ�������ӻ�����õ���ʽ��ʾ�Ȼ�þ���γɹ���Ϊ![]() ���ʴ�Ϊ��
���ʴ�Ϊ��![]() ��
��![]() ��
��

 ���Ž�������С״Ԫϵ�д�
���Ž�������С״Ԫϵ�д�