题目内容
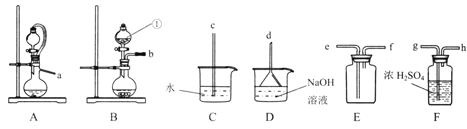
【题目】根据下图回答,下列说法错误的是( )

A. 电子经导线流入b电极
B. 若b极增重5.4 g时,燃料电池负极消耗CH4的体积为140 mL
C. 燃料电池中正极反应为O2+4e-+2H2O = 4OH-
D. 此装置用于电镀银时,一段时间后硝酸银溶液的浓度不变
【答案】B
【解析】A.通入甲醇的电极是负极,b是阴极,因此电子经导线流入b电极,A正确;B.若b极增重5.4 g,即析出银是0.05mol,转移0.05mol电子,根据电子得失守恒可知消耗甲醇是0.05mol÷8=0.00625mol,在标准状况下的体积是140mL,题干中没有注明条件,B错误;C.燃料电池中正极是氧气得到电子,发生还原反应,反应为O2+4e-+2H2O = 4OH-,C正确;D.电镀池中电解质溶液的浓度不变,因此此装置用于电镀银时,一段时间后硝酸银溶液的浓度不变,D正确,答案选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】法医常用马氏试砷法检验是否砒霜( As2O3)中毒,涉及的反应如下:
I:6Zn+As2O3+12HCl=6ZnCl2+2AsH3(砷烷)↑+3H2O
Ⅱ:2AsH3=2As(黑色砷镜)+3H2
(1)写出砷的基态原子价电子排布图______________。
(2)砷烷的空间结构为_______;砷烷中心原子杂化方式为________。
(3)砷烷同族同系列物质相关性质如下表:
NH3 | PH3 | AsH3 | SbH3 | |
熔点/℃ | -77.8 | -133.5 | -116.3 | -88 |
沸点/℃ | -34.5 | -87.5 | -62.4 | -18.4 |
从PH3→AsH3→SbH3熔沸点依次升高的原因是_________;NH3分子例外的原因是_______。
(4)第一电离能数据I(As)>I(Se),可能的原因是_____________。
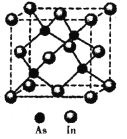
(5)砷与铟(In)形成的化合物(X)具有优良的光电性能,广泛应用于光纤通信用激光器,其晶胞结构如图所示,则其化学式为______;晶胞边长a= 666.67pm,则其密度为_____g/cm3(边长a可用![]() 近似计算,设NA=6.0×1023/mol)。
近似计算,设NA=6.0×1023/mol)。