题目内容
【题目】刑法修正案(八)中明确规定2011年5月1日“醉驾入刑”。
(1)酒精在人体肝脏内可转化为多种有害物质,有机物A是其中的一种,对A的结构进行如下
①通过样品的质谱分析测得A的相对分子质量为60;
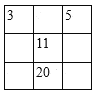
②经测定,有机物A的核磁共振氢谱示意图如图:

③对A的水溶液进行测定发现该溶液pH<7。根据以上分析,写出A的结构简式___________。
(2)工业酒精是含水约4%的液态乙醇。要在实验室中将工业酒精转化为无水酒精,请回答下列问题:
①下列做法中最不可取的是(填写代号)_ __________。
A.加入过量的生石灰后过滤
B.加入过量的生石灰后蒸馏
C.加入过量的生石灰后分液
②在该方法的实验步骤里,紧挨加热之前的操作是___________,并且对此要注意的问题是______________________。
③用酒精灯作热源,在加热的过程中要适时调整酒精灯的上下或左右位置,目的是_______________。
【答案】CH3COOH C 向冷凝管内通冷却水 水要从下口进、上口出 使蒸馏烧瓶内的支管口处保持某一恒温
【解析】
(1)根据①可知有机物A的相对分子质量为60;根据②可知有机物A中含有两种类型的氢原子,且两类氢原子个数比为1:3;根据③可判断有机物A含有羧基(-COOH);
(2)将工业酒精转化为无水酒精,加CaO与水反应后增大与乙醇的沸点差异;结合蒸馏实验需要的仪器及加热后馏分需要冷却分析;加热的过程中要适时调整酒精灯的上下或左右位置,控制蒸馏需要的温度。
(1)核磁共振氢谱中有几个峰就有几中氢原子,图2有2个峰,说明有2种氢原子,溶液pH<7,呈酸性,说明含有羧基,根据相对分子质量为60,60-45=13,另一个基团为甲基,故答案为:CH3COOH;
(2)①将工业酒精转化为无水酒精,加CaO与水反应后增大与乙醇的沸点差异,然后蒸馏即可,或加入过量的生石灰后,氢氧化钙在乙醇中溶解度较小,过滤分离,所以最不可取的为C,故答案为:C;
②紧挨加热之前的操作是向冷凝管内通冷却水,此时要注意水要从下口进、上口出,故答案为:向冷凝管内通冷却水;水要从下口进、上口出;
③加热的过程中要适时调整酒精灯的上下或左右位置,控制蒸馏需要的温度,即操作的目的为使蒸馏烧瓶内的支管口处保持某一恒温,故答案为:使蒸馏烧瓶内的支管口处保持某一恒温。

 阅读快车系列答案
阅读快车系列答案【题目】铅精矿可用于冶炼金属铅,其主要成分为PbS。
I.火法炼铅将铅精矿在空气中焙烧,生成PbO和SO2。
(1)用铅精矿火法炼铅的反应的化学方程式为_________。
(2)火法炼铅的废气中含低浓度SO2,可将废气通入过量氨水中进行处理,反应的离子方程式为:____。
II.湿法炼铅在制备金属铅的同时,还可制得硫磺,相对于火法炼铅更为环保。湿法炼铅的工艺流程如下:

已知:① 不同温度下PbCl2的溶解度如下表所示。
温度/℃ | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 1.00 | 1.42 | 1.94 | 2.88 | 3.20 |
② PbCl2为能溶于水的弱电解质,在Cl—浓度较大的溶液中,存在平衡: PbCl2(aq)+2Cl—(aq) ![]() PbCl42—(aq)
PbCl42—(aq)
(3)浸取液中FeCl3的作用是_________。
(4)结合信息判断,操作a为_________,以利于PbCl2的析出。
(5)将溶液3和滤液2分别置于如图所示电解装置的两个极室中,可制取金属铅并使浸取液中的FeCl3再生。
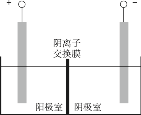
① 溶液3应置于______(填“阴极室”或“阳极室”)中。
② 简述滤液2电解后再生为FeCl3的可能原理:______。
③ 若铅精矿的质量为a g,铅浸出率为b,当电解池中通过c mol电子时,金属铅全部析出,铅精矿中PbS的质量分数的计算式为______。