题目内容
HA为酸性略强于醋酸的一元弱酸,在0.1 mol·L-1 NaA溶液中,离子浓度关系正确的是
| A.c(Na+)>c(A-)>c(H+)>c(OH-) |
| B.c(Na+)>c(OH-)>c(A-)>c(H+) |
| C.c(Na+)+c(OH-)=c(A-)+c(H+) |
| D.c(Na+)+c(H+)=c(A-)+c(OH-) |
D
解析试题分析:A、HA是弱酸,则在0.1 mol·L-1 NaA溶液中A-水解,溶液显碱性,则溶液中离子浓度大小关系是c(Na+)>c(A-)>c(OH-) >c(H+),A不正确;B、由于A-水解程度很小,所以溶液中c(A-)>c(OH-),B不正确;C、根据电荷守恒可知,c(Na+)+c(H+)=c(A-)+c(OH-),所以C不正确;D、根据电荷守恒可知,c(Na+)+c(H+)=c(A-)+c(OH-),D正确,答案选D。
考点:考查盐类水解、溶液中离子浓度大小比较

 名校课堂系列答案
名校课堂系列答案下列事实一定能证明HNO2是弱电解质的是( )
①常温下NaNO2溶液的pH大于7
②用HNO2溶液做导电实验,灯泡很暗
③HNO2和NaCl不能发生反应
④常温下0.1 mol·L-1 HNO2溶液的pH=2.1
⑤常温下pH=3的 HNO2溶液和pH=11的NaOH溶液等体积混合,pH小于7
⑥常温下pH=2的 HNO2溶液稀释至100倍,pH约为3.1
| A.①④⑥ | B.①②③④ | C.①④⑤⑥ | D.全部 |
下列有关“电离平衡”的叙述正确的是( )
| A.电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等 |
| B.电离平衡时,由于分子和离子的浓度不断发生变化,所以说电离平衡是静态平衡 |
| C.电离平衡是相对的、暂时的,外界条件改变时,平衡就会发生移动 |
| D.电解质达到电离平衡后,各种离子的浓度相等 |
关于NaHCO3溶液,下列表述不正确的是
| A.c (Na+)= c (HCO3-)+ c (CO32-)+ c (H2CO3) |
| B.c(Na+)+ c (H+)=" c" (HCO3-)+ c (CO32-)+ c (OH-) |
| C.HCO3-的水解程度大于HCO3-的电离程度 |
| D.c (H+) + c(H2CO3)=c (OH-)+ c(CO32-) |
在一定条件下,Na2CO3溶液中存在平衡CO32-+H2O HCO3-+OH-。下列说法错误的是
HCO3-+OH-。下列说法错误的是
A.稀释溶液, 增大 增大 |
| B.通入CO2,溶液pH减小 |
| C.升高温度,c(CO32-)减小 |
D.加入NaOH固体, 减小 减小 |
下列溶液一定呈中性的是
| A.pH=7的溶液 | B.c(H+)=c(OH-)的溶液 |
| C.非电解质溶于水得到的溶液 | D.由强酸、强碱等物质的量反应得到的溶液 |
已知醋酸、醋酸根离子在溶液中存在下列平衡:
CH3COOH+H2O 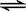 CH3COO—+H3O+ K1=1.75×10-5
CH3COO—+H3O+ K1=1.75×10-5
CH3COO—+H2O 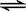 CH3COOH+OH— K2=5.71×10-10
CH3COOH+OH— K2=5.71×10-10
现有50 mL 0.2 mol·L-1醋酸与50 mL 0.2 mol·L-1醋酸钠混合制得溶液甲,下列叙述正确的是
| A.甲溶液的pH >7 |
| B.对甲进行微热,K1、K2同时增大 |
| C.若在甲中加入很少量的NaOH溶液,溶液的pH几乎不变 |
| D.若在甲中加入5 mL 0.1 mol·L-1的盐酸,则溶液中醋酸的K1会变大 |
下列有关电解质溶液中微粒的物质的量浓度关系正确的是( )
| A.pH=3的一元酸和pH=11的一元强碱等体积混合后的溶液中:c(OH-)=c(H+) |
| B.在0.1 mol·L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) |
| C.已知叠氮酸(HN3)与醋酸酸性相近,则在NaN3水溶液中离子浓度大小顺序为:c(Na+)>c(OH¯)>c(N3¯)>c(H+) |
| D.0.2 mol·L-1NaHCO3溶液中加入等体积0.1 mol·L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |