题目内容
20.下列图象最能反映2H2+O2═2H2O 反应过程中能量变化的是( )| A. |  | B. | 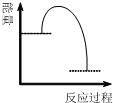 | C. | 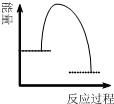 | D. |  |
分析 氢气和氧气燃烧生成水的反应是放热反应,所以反应物的总能量高于生成物的总能量,据此回答判断.
解答 解:氢气和氧气燃烧生成水的反应是放热反应,所以反应物的总能量高于生成物的总能量,反应活化分子需要吸收能量,变为活化分子,称为活化能,活化能要比反应的焓变数值小,只有图B符合.
故选B.
点评 本题考查学生化学反应的焓变和反应物、生成物能量之间的关系知识,注意知识的迁移应用是关键,难度中等.

练习册系列答案
 轻松暑假总复习系列答案
轻松暑假总复习系列答案
相关题目
6.下列有关分散系的叙述正确的是( )
| A. | 食盐溶液静置后会分层,下层比上层咸 | |
| B. | 悬浊液中一定不含直径小于10-9m的微粒 | |
| C. | 胶体区分于其他分散系的本质特征是胶体可以产生丁达尔效应 | |
| D. | 江河入海口处易形成三角洲,与胶体的性质有关 |
15.在密闭容中发生下列反应aA(g)?cC(g)+dD(g)△H=-m kJ/mol达到平衡后,将气体体积压缩到原来的一半,当再次达到平衡时,C的浓度为原平衡的1.7倍,下列叙述正确的是( )
| A. | 平衡向正反应方向移动了 | B. | A的转化率变大了 | ||
| C. | a<c+d | D. | △H值变大了 |
5.25℃时,水中存在电离平衡:H2O?H++OH-.下列叙述正确的是( )
| A. | 将水加热,KW增大,pH变小,液体显酸性 | |
| B. | 向水中通入少量HCl气体,c(H+)增大,KW不变 | |
| C. | 向水中加入少量NaOH固体,平衡逆向移动,c(OH-)减小 | |
| D. | 向水中加入少量纯碱,平衡正向移动,c(H+)增大 |
12.NH3 分子的空间构型是三角锥形,而不是正三角形的平面结构,解释该事实的充分理由是( )
| A. | NH3分子是极性分子 | |
| B. | 分子内3个N-H键的键长相等,键角相等 | |
| C. | NH3分子内3个N-H键的键长相等,3个键角都等于107° | |
| D. | NH3分子内3个N-H键的键长相等,3个键角都等于120° |
9.配制一定物质的量浓度的溶液时,会导致所配溶液浓度偏大的操作是( )
| A. | 在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中 | |
| B. | 定容摇匀后,发现液面低于刻度线,又加水到刻度线 | |
| C. | 用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理 | |
| D. | 定容时俯视刻度线 |
10.将20mL 0.5mol/L NaCl溶液A加水稀释至100mL的溶液B.下列溶液中,与B溶液中Cl-的物质的量浓度相同的是( )
| A. | 20 mL 0.5 mol/L KCl溶液 | B. | 200 mL 0.05 mol/L MgCl2溶液 | ||
| C. | 100 mL 0.1 mol/L AlCl3溶液 | D. | 50 mL 0.2 mol/L HCl溶液 |