题目内容
17.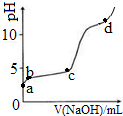 室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )
室温下,在0.2mol/LAl2(SO4)3溶液中,逐滴加入1.0mol/LNaOH溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图,下列说法正确的是( )| A. | a点,离子方程式为:Al3++3OH-→Al(OH)3↓ | |
| B. | a~b段,溶液pH增大,促进了氢氧化铝的碱式电离 | |
| C. | b~c段,加入的OH-主要用于生成Al(OH)3沉淀 | |
| D. | d点时,Al(OH)3沉淀开始溶解 |
分析 A.硫酸铝为强酸弱碱盐,水解显酸性;
B.a-b段,发生氢离子与碱中和反应,促进了氢氧化铝的酸式电离;
C.b-c段,pH变化不大;
D.c点后pH发生突变,NaOH过量.
解答 解:A.硫酸铝为强酸弱碱盐,水解显酸性,水解离子反应为Al3++3H2O?Al(OH)3+3H+,故A错误;
B.a-b段,加入NaOH溶液,消耗氢离子,促进了氢氧化铝的酸式电离,故B错误;
C.b-c段,pH变化不大,主要发生Al3++3OH-═Al(OH)3↓,则加入的OH-主要用于生成Al(OH)3沉淀,故C正确;
D.c点后pH发生突变,NaOH过量,Al(OH)3沉淀开始溶解,生成NaAlO2,碱性较强,而d点pH>10,NaOH远远过量,故D错误;
故选C.
点评 本题主要侧重盐类水解及复分解反应的考查,注意氢氧化铝的两性及图中c点pH突变为解答的关键,明确b→c段中铝离子过量,题目难度不大.

练习册系列答案
相关题目
8.元素的原子结构决定其性质和在周期表中的位置.下列说法正确的是( )
| A. | 元素原子的最外层电子数等于元素的最高化合价 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素 | |
| D. | 短周期元素(除0族元素外)从左到右,原子半径逐渐减小 |
5.下列实验装置设计正确,且能达到实验目的是( )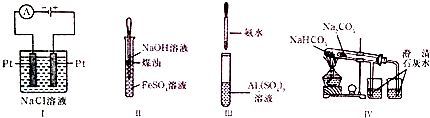

| A. | 实验Ⅰ:制备金属钠 | B. | 实验Ⅱ:制取Fe(OH)2并观察其颜色 | ||
| C. | 实验Ⅲ:制取NaAlO2 | D. | 实验Ⅳ:比较两种物质的热稳定性 |
12.下列鉴别方法不可行的是( )
| A. | 仅用氨水即可鉴别NaCl、AlBr3、FeI2、AgNO3四种溶液 | |
| B. | 用燃烧法鉴别环己醇、苯和四氯化碳 | |
| C. | 用烧碱溶液鉴别地沟油、甘油和石油 | |
| D. | 用新制氯水鉴别碘的淀粉溶液、含石蕊的烧碱溶液、硫酸铜溶液等三种蓝色溶液 |
9.下列反应过程中,同时有离子键、极性共价键和非极性共价键的断裂和形成的反应是( )
| A. | NH4Cl→NH3↑+HCl↑ | B. | NH3+CO2+H2O→NH4HCO3 | ||
| C. | 2NaOH+Cl2→NaCl+NaClO+H2O | D. | 2Na2O2+2CO2→2Na2CO3+O2 |
7.分子式为C5H12O其中含有2个甲基的醇与分子式为C5H10O2的酸发生酯化反应得到的有机物可能的结构有(不包括立体异构)( )
| A. | 24种 | B. | 16种 | C. | 12种 | D. | 8种 |
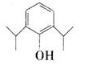
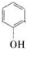 +2CH2=C(CH3)2→
+2CH2=C(CH3)2→
 .
.