题目内容
已知反应KClO3+6HCl═KCl+3Cl2↑+3H2O.下列判断正确的是( )
| A、KClO3被氧化 |
| B、氧化剂与还原剂之比为1:6 |
| C、氧化产物是Cl2 |
| D、HCl在化学反应中只能作还原剂 |
考点:氧化还原反应
专题:氧化还原反应专题
分析:该反应中氯酸钾在Cl元素化合价由+5价变为0价、HCl中Cl元素化合价由-1价变为0价,所以氯酸钾是氧化剂、部分氯化氢是还原剂,据此分析解答.
解答:
解:该反应中氯酸钾在Cl元素化合价由+5价变为0价、HCl中Cl元素化合价由-1价变为0价,
A.氯酸钾是氧化剂,在反应中被还原,故A错误;
B.该反应中有
的HCl作还原剂,所以氧化剂和还原剂的物质的量之比为1:5,故B错误;
C.该反应中氯气既是氧化产物又是还原产物,故C正确;
D.该反应中HCl部分Cl化合价升高、部分化合价不变,所以HCl既作还原剂又起酸的作用,故D错误;
故选C.
A.氯酸钾是氧化剂,在反应中被还原,故A错误;
B.该反应中有
| 5 |
| 6 |
C.该反应中氯气既是氧化产物又是还原产物,故C正确;
D.该反应中HCl部分Cl化合价升高、部分化合价不变,所以HCl既作还原剂又起酸的作用,故D错误;
故选C.
点评:本题考查了氧化还原反应,根据元素化合价变化来分析解答,注意该反应中HCl的作用,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
既能与稀硫酸反应,又能与NaOH溶液反应,且都有气体放出的是( )
| A、NaHCO3 |
| B、Al |
| C、Fe |
| D、Al2O3 |
t℃时,水的离子积为KW,该温度下将a mol?L-1一元酸HA与b mol?L-1一元碱BOH等体积混合,要使混合液呈中性,必要的条件是( )
| A、混合液的pH=7 | ||
B、混合液中c(H+)=
| ||
| C、a=b | ||
| D、混合液中c(B+)=c(A-)+c(OH-) |
下列文字表述与对应的离子方程式正确的是( )
A、用惰性电极电解饱和氯化钠溶液:2Cl-+2H+
| ||||
| B、在H2O2溶液中,滴加FeCl3溶液产生气泡:2H2O2+2Cl-═2H2O+O2↑+Cl2↑ | ||||
| C、利用腐蚀法制作印刷线路板:Fe3++Cu═Fe2++Cu2+ | ||||
| D、向AgC1悬浊液中滴加Na2S溶液,白色沉淀变成黑色2AgCl+S2-═Ag2S+2Cl- |
下列表示对应化学反应的离子方程式或化学方程式正确的是( )
| A、向NH4HSO4的稀溶液中逐滴加入Ba(OH)2溶液至刚好沉淀完全:NH4++H++SO42-+Ba2++2OH-═NH3?H2O+BaSO4↓+H2O | ||||
| B、酸性高锰酸钾溶液与H2O2溶液混合:2MnO4-+3H2O2+6H+═2Mn2++6H2O+O2↑ | ||||
C、用铜作电极电解饱和食盐水:2Cl-+2H2O
| ||||
D、以下有机物在碱性条件下水解的化学方程式:BrCH2- -OOCH+3NaOH -OOCH+3NaOH
 ONa+HCOONa+NaBr ONa+HCOONa+NaBr |
下列关于化工生产原理的叙述中,不符合目前工业生产实际的是( )
| A、为充分利用原料,在氯碱工业、合成氨工业和纯碱工业的生产过程中均采用了原料循环使用的工艺 |
| B、通过电解Fe2O3-SiO2-CaO的熔融液(1600℃)来大规模地冶炼铁 |
| C、生产重要的化工原料氯化氢是将氯气在氢气中点燃充分燃烧来获得的 |
| D、用不同的碱液来吸收制酸工业中的尾气,其目的都包含着既防止有害气体的排放,同时又生产出一些有用的化工辅料这样一种“绿色化学”的理念 |
鉴别Clˉ、Brˉ、Iˉ三种离子,宜选用的试剂组是( )
| A、溴水和淀粉溶液 |
| B、硝酸银溶液和稀硝酸 |
| C、氯水和四氯化碳 |
| D、氯水和碘化钾淀粉溶液 |
2014年5月21日,中俄签订了30年天然气供应合同,成为我国得到清洁能源的主要来源.天然气的主要成分是( )
| A、CH4 |
| B、C2H4 |
| C、CO |
| D、H2 |
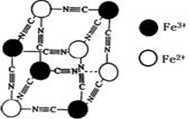 分析化学中常用X射线研究晶体结构.
分析化学中常用X射线研究晶体结构.