题目内容
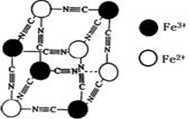 分析化学中常用X射线研究晶体结构.
分析化学中常用X射线研究晶体结构.有一种晶体KxFey(CN)z,其中Fe2+、Fe3+、CN-的排布如图所示.每隔一个立方体,在立方体的中心含有一个K+(未画出).
(1)晶体的化学式可表示为
(2)1molKxFey(CN)z晶体中含π键
考点:晶胞的计算
专题:化学键与晶体结构
分析:(1)利用均摊法计算出各种微粒在晶胞中数目;
(2)根据晶胞中C≡N数目判断.
(2)根据晶胞中C≡N数目判断.
解答:
解:(1)Fe2+数=Fe3+数=4×
=
,即化学式中含Fe数目=
;CN-位于棱,数目=12×
,两个晶胞含有一个K+,一个晶胞含有
个K+,即化学式可写为:KFe2(CN)6,故答案为:KFe2(CN)6;
(2)1molCN-中含有2molπ键,故1molK1Fe2(CN)6晶体中含有2mol×6=12molπ键,故答案为:12.
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 4 |
| 1 |
| 2 |
(2)1molCN-中含有2molπ键,故1molK1Fe2(CN)6晶体中含有2mol×6=12molπ键,故答案为:12.
点评:本题考查物质结构与性质,涉及化学键和晶胞计算等知识点,难度较小,解题时要注意均摊法的应用.

练习册系列答案
相关题目
已知反应KClO3+6HCl═KCl+3Cl2↑+3H2O.下列判断正确的是( )
| A、KClO3被氧化 |
| B、氧化剂与还原剂之比为1:6 |
| C、氧化产物是Cl2 |
| D、HCl在化学反应中只能作还原剂 |