题目内容
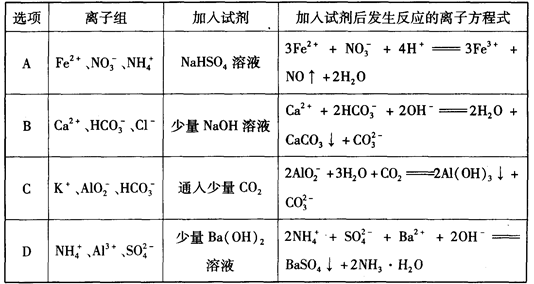
常温,相应条件下,下列各组离子一定能大量共存的是
| A.c(Al3+)=0.1mol/L的溶液中:Na+、K+、AlO2-、OH- |
| B.无色溶液中:K+、CH3COO-、HCO3-、MnO4- |
C.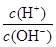 =1×1014的溶液:Ba2+、Na+、SO32-、NO3- =1×1014的溶液:Ba2+、Na+、SO32-、NO3- |
| D.通入足量CO2后所含离子还能大量共存的是:K+、Ca2+、NO3-、Cl- |
D
试题分析:A、AlO2-与铝离子可以发生又水解,错误;B、MnO4-是有颜色:紫色,错误;C、
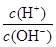 =1×1014的溶液是强酸性溶液,硝酸根离子在强酸性条件下可以氧化亚硫酸根离子成硫酸根离子,而本身被还原成氮的氧化物。错误;D、通入足量CO2后可以跟钙离子形成碳酸氢钙,不影响钙离子的量。正确。
=1×1014的溶液是强酸性溶液,硝酸根离子在强酸性条件下可以氧化亚硫酸根离子成硫酸根离子,而本身被还原成氮的氧化物。错误;D、通入足量CO2后可以跟钙离子形成碳酸氢钙,不影响钙离子的量。正确。
练习册系列答案
相关题目