题目内容
【题目】50 mL浓H2SO4溶液(足量)中加入3.2 g Cu,在加热条件下充分反应:
(1)将题干中反应后的溶液稀释到500 mL,取出50 mL,并向取出液中加入足量的BaCl2溶液,得到沉淀19.81 g,则原浓硫酸的物质的量浓度为____。
(2)若题干中浓硫酸的物质的量浓度为a mol/L,投入足量的铜片加热,充分反应后,被还原的硫酸的物质的量n(H2SO4)___0.025a mol(填“等于”、“大于”或“小于”)。
(3)反应消耗的H2SO4的物质的量是____,生成SO2的体积为(标准状况下)_____mL。
【答案】小于 18 0.1 1120
【解析】
Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O中,2mol H2SO4(浓)被消耗,发生还原反应的H2SO4为1mol,产生1molSO2;反应后的溶液中满足n(H2SO4)=[n(
CuSO4+SO2↑+2H2O中,2mol H2SO4(浓)被消耗,发生还原反应的H2SO4为1mol,产生1molSO2;反应后的溶液中满足n(H2SO4)=[n(![]() )+n(SO2)] mol关系;随着反应的进行,浓硫酸逐渐变为稀硫酸,而稀硫酸与铜不反应,反应停止。
)+n(SO2)] mol关系;随着反应的进行,浓硫酸逐渐变为稀硫酸,而稀硫酸与铜不反应,反应停止。
(1)根据反应方程式,硫酸一部分起酸性作用,一部分起氧化剂作用,因此根据硫元素守恒,n(H2SO4)=[n(![]() )+n(SO2)] mol=(
)+n(SO2)] mol=( ![]() +
+![]() )mol=0.9mol,因此c(H2SO4)=
)mol=0.9mol,因此c(H2SO4)=![]() =18mol·L-1;
=18mol·L-1;
(2)在Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O中,被还原的硫酸的物质的量是参加反应的硫酸的一半。硫酸不足,铜过量,因此根据硫酸进行计算,被还原硫酸的物质的量为50×10-3×
CuSO4+SO2↑+2H2O中,被还原的硫酸的物质的量是参加反应的硫酸的一半。硫酸不足,铜过量,因此根据硫酸进行计算,被还原硫酸的物质的量为50×10-3×![]() ×amol=0.025amol,但铜只与浓硫酸反应,随着反应的进行,硫酸浓度降低,转化成稀硫酸,反应停止,即被还原的稀硫酸的物质的量小于0.025amol;
×amol=0.025amol,但铜只与浓硫酸反应,随着反应的进行,硫酸浓度降低,转化成稀硫酸,反应停止,即被还原的稀硫酸的物质的量小于0.025amol;
(3)发生的反应是Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,因为硫酸是过量的,因此根据铜进行计算,n(Cu)=
CuSO4+SO2↑+2H2O,因为硫酸是过量的,因此根据铜进行计算,n(Cu)=![]() =0.05mol,消耗硫酸的物质的量为n(H2SO4)=2n(Cu)=2×0.05mol=0.1mol,产生V(SO2)=0.05mol×22.4L/mol=1.12L,即1120mL。
=0.05mol,消耗硫酸的物质的量为n(H2SO4)=2n(Cu)=2×0.05mol=0.1mol,产生V(SO2)=0.05mol×22.4L/mol=1.12L,即1120mL。

 名校课堂系列答案
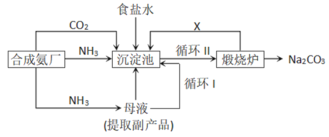
名校课堂系列答案【题目】锰锌铁氧体是应用广泛的高性能磁性材料。现以akg废旧碱性锌锰电池为原料(含锰元素的物质:MnO2占b%,MnOOH占c%)制备锰锌铁氧体,主要流程如下:
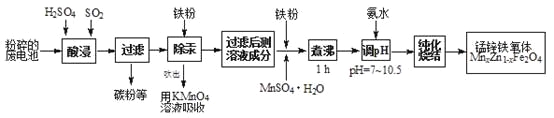
(1)酸浸废电池时,被溶解生成Zn2+的物质有______,SO2的作用是_____(填字母编号)。
A.漂白剂 | B.沉淀剂 | C.氧化剂 | D.还原剂 |
(2)除汞是以氮气为载体吹入滤液带出汞蒸汽,经KMnO4溶液吸收而实现的。如图是KMnO4溶液处于不同pH时对应的单位时间Hg去除率变化图,图中物质为Hg与MnO4-在该pH范围反应的主要产物。
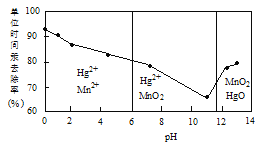
①pH<6时反应的离子方程式为___________。
②汞的去除速率随pH变化的规律是_________。
(3)锌锰干电池中MnO2可以用碳酸锰在空气中煅烧制得。
已知25℃,101 kPa时:2MnO(s)+O2(g)=2MnO2(s) H=-272.0 kJ/mol
MnCO3(s)=MnO(s)+CO2(g) H=+116.6 kJ/mol
碳酸锰在空气中煅烧反应生成MnO2的热化学方程式是_______________。
(4)x=0.2的锰锌铁氧体具有较高的饱和磁场强度,该锰锌铁氧体的组成用氧化物形式(最简整数比)表示为____________。若制得这种锰锌铁氧体的质量为100 kg,在制取过程中不考虑损耗,需补充硫酸锰晶体(MnSO4·H2O)_________kg。(只列出计算式)