题目内容
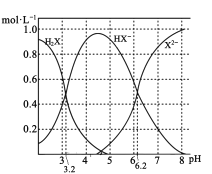
【题目】25 C时,H2SO3的pKa1、pKa2(pK= -lgK)分别为1.89、7.20, NH3·H2O的pKb为4.72。常温时,下列指定溶液中粒子物质的量浓度关系正确的是
A.pH=3的H2SO3溶液中,c(HSO3 -) +2c(SO3-)=1 ×10-3 mol·L-1
B.0.1 mol·L-1H2SO3溶液用NaOH溶液滴定至pH =7.20, c( HSO3 ) =2c(SO3- )
C.0.1 mol.L-1H2SO3溶液用氨水滴定至pH=7.0, c(NH4+) =c(HSO3-) +c(SO32- )
D.0.1 mol·L-1NH4HSO3溶液中: c(NH4+ ) >c(H+) >c( NH3·H2O)
【答案】D
【解析】
A. pH=3的H2SO3溶液中,根据电荷守恒可知c(H+)= c(HSO3 -) +2c(SO3-)+ c(OH-)=1 ×10-3 mol·L-1,故A错误;
B. pH =7.20,即溶液中c(H+)=1×10-7.20 mol·L-1,H2SO3的Ka2=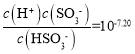 ,则
,则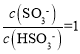 ,即c( HSO3 ) =c(SO3-),故B错误;
,即c( HSO3 ) =c(SO3-),故B错误;
C. 溶液中存在电荷守恒c(H+)+c(NH4+)= c(HSO3-)+2c(SO3-)+ c(OH-),pH=7.0,则c(H+)=c(OH-),所以c(NH4+)= c(HSO3 -) +2c(SO3-),故C错误;
D. 0.1 mol·L-1NH4HSO3溶液中存在:NH4++H2O NH3·H2O+ H+,水解是微弱的,所以c(NH4+)> c(NH3·H2O);同时存在亚硫酸氢根的水解和电离,亚硫酸氢根的水解平衡常数为![]() ,则亚硫酸氢根的电离程度大于水解程度,所以由于亚硫酸氢根的存在会使溶液显酸性,铵根的水解平衡常数为
,则亚硫酸氢根的电离程度大于水解程度,所以由于亚硫酸氢根的存在会使溶液显酸性,铵根的水解平衡常数为![]() ,小于HSO3-的电离常数,所以c(NH4+ ) >c(H+) >c( NH3·H2O),故D正确;
,小于HSO3-的电离常数,所以c(NH4+ ) >c(H+) >c( NH3·H2O),故D正确;
故答案为D。

 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案