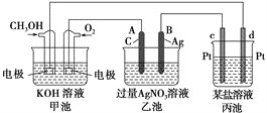
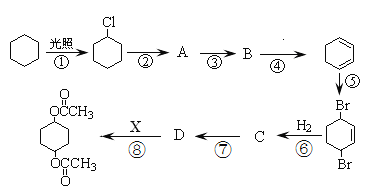
题目内容
【题目】随着人类对温室效应和资源短缺等问题的重视,如何降低大气中CO2的含量及有效地开发利用CO2,引起了各国的普遍重视。
⑴目前工业上有一种方法是用CO2来生产燃料甲醇。为探究反应原理,现进行如下实验,在体积为1 L的密闭容器中,充入1mol CO2和3mol H2,一定条件下发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
CH3OH(g)+H2O(g) △H=-49.0kJ/mol,测得CO2和CH3OH(g)的浓度随时间变化如图所示。
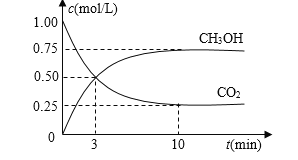
①从反应开始到平衡,氢气的平均反应速率v(H2)=_____mol/(L·min)。
②该反应的平衡常数表达式为K=_________。
③下列措施中能使n(CH3OH)/n(CO2)增大的是___________。
A.升高温度 B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离 D.再充入1mol CO2和3mol H2
⑵有人提出,可以设计反应2CO(g)=2C(s)+O2(g) 通过其自发进行来消除CO的污染。该方案_______(填“是”、“否”)可行,理由是:_______。
【答案】0.225 ![]() CD 否 该反应△H>0、△S<0,因而△G>0,不能自发进行
CD 否 该反应△H>0、△S<0,因而△G>0,不能自发进行
【解析】
(1)①根据v=![]() 计算;
计算;
②根据平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积计算;
③要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动;
(2)根据△G的大小判断反应能否进行。
(1)①利用三段式解题法计算
CO2(g)+3H2(g)CH3OH(g)+H2O(g),
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
从反应开始到平衡,氢气的平均反应速率v(H2)=![]() =0.225 molL-1min-1;
=0.225 molL-1min-1;
②平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则K=![]() ;
;
③要使n(CH3OH)/n(CO2)增大,应使平衡向正反应方向移动;A.因正反应放热,升高温度平衡向逆反应方向移动,则n(CH3OH)/n(CO2)减小,故A错误;B.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,n(CH3OH)/n(CO2)不变,故B错误;C.将H2O(g)从体系中分离,平衡向正反应方法移动,n(CH3OH)/n(CO2)增大,故C正确;D.再充入1mol CO2和3mol H2,等效于在原来基础上缩小体积一半,压强增大,平衡向正反应方向移动,则n(CH3OH)/n(CO2)增大,故D正确;故答案为CD;
(2)已知反应2CO=2C+O2的△H>0、△S<0,则△G=△H-T△S>0,反应是一个焓增、熵减的反应,任何情况下不能自发进行。

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案