题目内容
下列说法正确的是( )
| A.增大压强,化学反应速率一定增大 |
| B.化学反应速率为反应时间内反应物浓度的增加或者生成物浓度的减少 |
| C.升高温度,化学反应速率一定增大 |
| D.加入反应物,化学反应速率增大 |
C
解析试题分析:A.对于有气体参加的反应,若是通过改变容器的容积来增大压强,化学反应速率一定增大。若是容器的容积不变,而加入了惰性气体,则增大压强,化学反应速率不变。错误。B.化学反应速率是衡量化学反应进行的快慢程度的物理量。通常是用反应时间内反应物浓度的减少或者生成物浓度的增加来表示的。错误。C.升高温度,分子的能量增加,分子间的有效碰撞次数增加,所以化学反应速率一定增大。正确。D.若是加入固体或纯液体状态的反应物,则化学反应速率不变。错误。
考点:考查温度、压强等外界条件对化学反应速率的影响的知识。

已知分解1 mol H2O2 放出热量98KJ,在含少量I-的溶液中,H2O2的分解机理为:
H2O2+ I- →H2O +IO- 慢 H2O2+ IO-→H2O +O2+ I- 快
下列有关反应的说法正确的是( )
| A.反应的速率与I-的浓度有关 | B.IO-也是该反应的催化剂 |
| C.反应活化能等于98KJ·mol-1 | D.v(H2O2)=v(H2O)=v(O2) |
在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应如下:2A(g)+B(g) 2D(g) △H=-QKJ·mol-1。相关条件和数据见下表:
2D(g) △H=-QKJ·mol-1。相关条件和数据见下表:
| 实验编号 | 实验Ⅰ | 实验Ⅱ | 实验Ⅲ |
| 反应温度/℃ | 800 | 800 | 850 |
| 达平衡时间/min | 40 | 10 | 30 |
| c(D)平衡/mol·L-1 | 0.5 | 0.5 | 0.15 |
| 反应的能量变化/KJ | Q1 | Q2 | Q3 |
A.可用压强或密度是否发生变化判断上述反应是否达到平衡
B.实验Ⅱ可能隐含的条件是使用催化剂,实验Ⅲ达平衡时υ(D)为0.01mol·L-1·min-1
C.由表中信息可知Q>O,并显有Q3<Q2=Q1=Q
D.实验Ⅰ达平衡后,恒温下再向容器中通入1molA和1molD,达平衡时c(D)为1.0mol·L-1。
在容积为2 L的恒容的密闭容器中,一定温度下,发生反应:aM(g)+bN(g) cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
cQ(g)。气体M、N、Q的物质的量随时间的变化如图所示,则下列叙述正确的是( )
| A.该温度下此反应的平衡常数的值K=25/4 |
| B.该反应前5 min的平均速率:v(N)=0.002 mol·L-1·min-1 |
| C.在5 min时,再向体系中充入少量He,重新达到平衡前v(正)>v(逆) |
| D.若开始时向容器中充入2mol M和1mol N,达到平衡时,M的体积分数小于50% |
下列说法正确的是( )
| A.增大压强,化学反应速率一定增大 |
| B.化学反应速率为反应时间内反应物浓度的增加或者生成物浓度的减少 |
| C.升高温度,化学反应速率一定增大 |
| D.加入反应物,化学反应速率增大 |
在5L的密闭容器中进行下述反应 30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是
30S内,NO增加了0.3mol,则在30S内,该反应的平均反应速率正确的是
| A.V(O2)=0.01mol·L-1·s-1 | B.V(NO)=0.08mol·L-1·s-1 |
| C.V(H2O)=0.01mol·L-1·s-1 | D.V(NH3)=0.002mol·L-1·s-1 |
在密闭容器中进行下列反应:M(气)+N(气) R(气)+2L此反应符合下面图象,下列叙述正确的是( )
R(气)+2L此反应符合下面图象,下列叙述正确的是( )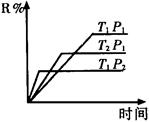
| A.正反应吸热,L是气体 |
| B.正反应吸热,L是固体 |
| C.正反应放热,L是气体 |
| D.正反应放热,L是固体或液体 |
如下图所示,图Ⅰ是恒压密闭容器,图Ⅱ是恒容密闭容器。当其它条件相同时,在Ⅰ、Ⅱ中分别加入2 mol X和2 mol Y,开始时容器的体积均为V L,发生如下反应并达到平衡状态(提示:物质X、Y的状态均未知,物质Z的状态为气态):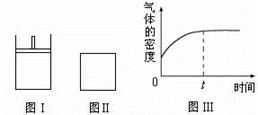
2X(?)+ Y(?) a Z(g)。
a Z(g)。
此时Ⅰ中X、Y、Z的物质的量之比为1∶3∶2。下列判断正确的是
| A.物质Z的化学计量数a = 2 |
| B.若X、Y均为气态,则在平衡时X的转化率:Ⅰ> Ⅱ |
| C.若Ⅱ中气体的密度如图Ⅲ所示,则X、Y都为气态 |
| D.若X为固态、Y为气态,则Ⅰ、Ⅱ中从开始到平衡所需的时间:Ⅰ>Ⅱ |
在一恒容的密闭容器中充入0.1 mol/L CO2、0.1 mol/L CH4,在一定条件下发生反应:CH4(g)+CO2(g)  2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是
2CO(g)+2H2(g),测得CH4平衡时转化率与温度、压强关系如图,下列有关说法不正确的是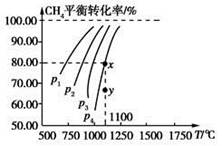
| A.上述反应的ΔH<0 |
| B.压强:p4>p3>p2>p1 |
| C.1100 ℃时该反应平衡常数为1.64 |
| D.压强为p4时,在y点:v正>v逆 |