题目内容
【题目】利用待测溶液和指定的试剂设计实验,不能达到实验目的的是
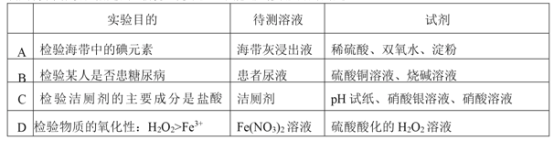
A.AB.BC.CD.D
【答案】D
【解析】
A.向海带灰浸出液中加入稀硫酸酸化,再加入双氧水,溶液由无色变为黄色,可初步判断海带中含有碘元素,再加入淀粉,溶液变蓝色,可确定海带中含有碘元素,故A正确;
B.先用硫酸铜溶液与过量烧碱溶液反应,得到新制的氢氧化铜悬浊液。将其与患者尿液混合,加热,若产生砖红色沉淀则说明患糖尿病,反之则不是,故B正确;
C.用pH试纸测得洁厕剂显强酸性,取少量洁厕剂滴入硝酸钡溶液中,无明显现象,再加入硝酸银溶液,若有白色沉淀生成则说明洁厕剂中含有氯离子,综上可检验洁厕剂的主要成分是盐酸,故C正确;
D.硝酸的氧化性强于过氧化氢,用硫酸酸化的过氧化氢溶液和硝酸亚铁反应时,硝酸作为氧化剂,故不能说明过氧化氢的氧化性强于铁离子,故D错误;
故答案选:D。

练习册系列答案
 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案
相关题目