题目内容
【题目】依据事实,回答下列问题。
(1)在25℃、101kPa时,1.0gC8H18(l,辛烷)燃烧生成CO2(g)和H2O(l),放出48.40kJ的热量,则C8H18(l)的燃烧热为___kJ/mol。
(2)已知N2(g)+2O2(g)=2NO2(g);ΔH=+67.7kJ/mol,N2H4(g)+O2(g)=N2(g)+2H2O(g);ΔH=-534kJ/mol,根据盖斯定律写出肼(N2H4)与NO2完全反应生成氮气和气态水的热化学方程式____。
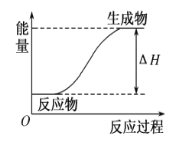
(3)某反应过程中的能量变化如图所示,则该反应是____(填“放热”或“吸热”)反应,判断依据是____。
(4)已知:2NH3(g)+3Cl2(g)=N2(g)+6HCl(g) ΔH=–462kJmol-1
![]() ,
,![]()
则断开1molH–N键与断开1molH–Cl键所需能量相差约为_____kJ。
【答案】5517.60kJ/mol 2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H= -1135.7kJmol-1 吸热反应 反应物的总能量低于生成物的总能量 41
【解析】
(1)在25℃时,101kPa下,1g辛烷燃烧生成二氧化碳和液态水放出48.40kJ的热量,则1mol辛烷即114g辛烷燃烧生成二氧化碳和液态水放出5518kJ的热量,所以其燃烧热为5517.60kJ/mol;
(2)①N2(g)+2O2(g)=2NO2(g),△H=+67.7kJmol-1;②N2H4(g)+O2(g)=N2(g)+2H2O(g),△H=-534kJmol-1,将方程式2×②-①得2N2H4(g)+2NO2(g)=3N2(g)+4H2O(g)△H=2(-534kJmol-1)-(+67.7kJmol-1)=-1135.7kJmol-1;
(3)由能量变化图可知,反应物的总能量低于生成物的总能量,则该反应是吸热反应;
(4)断开1molH–N键与断开1molH–Cl键所需能量分别为x kJ、y kJ,根据△H=反应物键能之和-生成物键能之和,可知:-462=6x+3×243-(945+6y),解得:x-y=-41,即断开1molH–N键与断开1molH–Cl键所需能量相差为41kJ。

 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案【题目】氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题:
(1)氟代硼酸钾中各元素原子的第一电离能大小顺序是F>O>____________。基态K+电子占据最高能级的电子云轮廓图为________形。
(2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是_______,中心原子的杂化形式为_______。NaBH4中存在_____(填标号)。
a. 离子键 b.氢键 c.σ键 d.π键
(3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为________,其中Be的配位数为_______。
(4)第三周期元素氟化物的熔点如下表:
化合物 | NaF | MgF2 | AlF3 | SiF4 | PF5 | SF6 |
熔点/℃ | 993 | 1261 | 1291 | -90 | -83 | -50.5 |
解释表中氟化物熔点变化的原因:_____________________。
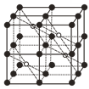
(5)CaF2的一种晶胞如图所示。Ca2+占据F-形成的空隙,其空隙率是________。若r(F-)=xpm,r(Ca2+)=ypm,设阿伏加德罗常数的值为NA,则CaF2的密度ρ=_________ g·cm-3(列出计算表达式)。
【题目】氮的氧化物(NOx)是大气污染物之一,工业上在一定温度和催化剂条件下用NH3将NOx还原生成N2,某同学在实验室中对NH3与NOx反应进行了探究。回答下列问题:
(1)氨气的制备
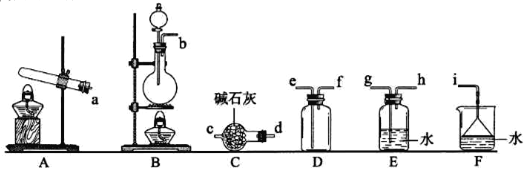
①氨气的发生装置可以选择上图中的________,反应的化学方程式为______________。
②预收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→______(按气流方向,用小写字母表示)。
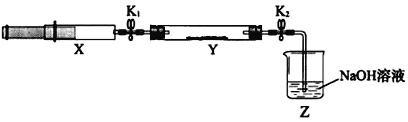
(2)氨气与二氧化氮的反应将上述收集到的NH3充入注射器X中,硬质玻璃管Y中加入少量催化剂,充入NO2(两端用夹子K1、K2夹好)。在一定温度下按图示装置进行实验。
操作步骤 | 实验现象 | 解释原因 |
打开K1,推动注射器活塞,使X中的气体缓慢通入Y管中 | ①Y管中_____________ | ②反应的化学方程式 ____________ |
将注射器活塞退回原处并固定,待装置恢复到室温 | Y管中有少量水珠 | 生成的气态水凝集 |
打开K2 | ③_______________ | ④______________ |