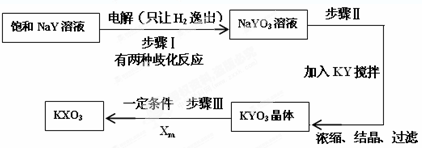
��Ŀ����
13��ijͬѧ����ͼ��ʾװ����ȡ�屽�������飮��֪��������Ϊ��ɫҺ�壬������ˮ���е�Ϊ38.4�棬�۵�Ϊ-119�森
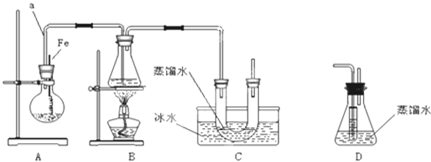
��Ҫʵ�鲽�����£�
����װ��װ�ã�����������ԣ�
������ƿ�м���һ��������Һ�壬����ƿ�м����Ҵ����Ը��ڽ������ܿڴ�����U���м�������ˮ��ס�ܵף���ˮ���м����ˮ��
�۽�Aװ���еĴ���˿С�����²��뱽��Һ��Ļ��Һ�У�
�ܵ�ȼBװ���еľƾ��ƣ���С������ƿ����10���ӣ�
����д���пհף�
��1����д��Aװ������������A��
 +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$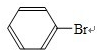 +HBr��
+HBr����2����������ټ���װ�������Եľ���������������D����װ��װ�ú���U���ұߵ��ܿ�����һ���ܴ��н��ܵIJ������ܣ������ܷ���ˮ���£�������ƿ�������ܿڴ������ݲ�����ֹͣ���Ⱥ�����һ��ˮ��������֤��װ�õ����������ã�
��3��Cװ����U���ڲ�������ˮ��ס�ܵ��������ܽ������廯�����壬��ֹ�廯�⼰�����ݳ���Ⱦ������
��4����Ӧ��Ϻ�U����Һ��ֲ㣬���������£���ϻ��£��㣮
��5��Ϊ֤����ͱ���������Ӧ��ȡ����Ӧ�����Ǽӳɷ�Ӧ����ѧ����װ��D����װ��B��Cֱ����A�������²���ʵ�飮
��װ��D����ƿ�У�С�Թ��ڵ�Һ���DZ��������Ȼ�̼��������һ�ַ��������Լ������ƣ�������Ҫ���������ջӷ���������������
�ڷ�Ӧ������ƿ�еμӣ�����һ�ַ��������Լ������ƣ���������Һ������ɫʯ����Һ������֤���÷�ӦΪȡ����Ӧ�е���ɫ��������������ɫʯ����Һ��죩��
���� ��1��������������ʱ���Ժ��巢��ȡ����Ӧ����屽��
��2������ѹǿ����������ж�װ�������ԣ�
��3����������ǿ�ᣬˮ������ֹ���ʵ��������ˮ������ã�
��4����������ܶȴ���ˮ��
��5����ͼ��֪��A�з��� +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��װ��D����ƿ��С�Թ��ڱ��������Ȼ�̼�������壬��ƿ�ڵ�Һ��Ϊˮ������HBr���壬Ȼ��μ����������������ӣ�
+HBr��װ��D����ƿ��С�Թ��ڱ��������Ȼ�̼�������壬��ƿ�ڵ�Һ��Ϊˮ������HBr���壬Ȼ��μ����������������ӣ�
��� �⣺��1��������������ʱ���Ժ��巢��ȡ����Ӧ����屽��������Ӧ��ԭ������ʽΪ�� +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��
+HBr��
�ʴ�Ϊ�� +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��
+HBr��
��2��������м���װ�������Եľ�����������װ��װ�ú���U���ұߵ��ܿ�����һ���ܴ��н��ܵIJ������ܣ������ܷ���ˮ���£�������ƿ�������ܿڴ������ݲ�����ֹͣ���Ⱥ�����һ��ˮ��������֤��װ�õ����������ã�
�ʴ�Ϊ����װ��װ�ú���U���ұߵ��ܿ�����һ���ܴ��н��ܵIJ������ܣ������ܷ���ˮ���£�������ƿ�������ܿڴ������ݲ�����ֹͣ���Ⱥ�����һ��ˮ��������֤��װ�õ����������ã�
��3���廯�⼫������ˮ���γɵ���������ǿ�ᣬˮ������ֹ�ӷ�����HBr���������ˮ������ã�
�ʴ�Ϊ���ܽ������廯�����壬��ֹ�廯�⼰�����ݳ���Ⱦ������
��4����������ܶȴ���ˮ�����Է�Ӧ��Ϻ�U����Һ��ֲ㣬���������²㣬
�ʴ�Ϊ���£�
�������ӷ�Ӧ�����ɸ����������ȡ����Ӧ����HBr��
��5����ͼ��֪��A�з��� +Br2$\stackrel{Fe}{��}$
+Br2$\stackrel{Fe}{��}$ +HBr��װ��D����ƿ��С�Թ��ڱ��������Ȼ�̼�������壬��ƿ�ڵ�Һ��Ϊˮ������HBr���壬Ȼ��μ����������������ӣ����Ԣ�װ��D����ƿ�У�С�Թ��ڵ�Һ���� CCl4������Ҫ���������ջӷ����������������ڷ�Ӧ������ƿ�еμ� ��������Һ������ɫʯ����Һ������ ��������Һ������ɫʯ����Һ��֤���÷�ӦΪȡ����Ӧ��
+HBr��װ��D����ƿ��С�Թ��ڱ��������Ȼ�̼�������壬��ƿ�ڵ�Һ��Ϊˮ������HBr���壬Ȼ��μ����������������ӣ����Ԣ�װ��D����ƿ�У�С�Թ��ڵ�Һ���� CCl4������Ҫ���������ջӷ����������������ڷ�Ӧ������ƿ�еμ� ��������Һ������ɫʯ����Һ������ ��������Һ������ɫʯ����Һ��֤���÷�ӦΪȡ����Ӧ��
�ʴ�Ϊ�����������Ȼ�̼�������ջӷ�����������������������Һ������ɫʯ����Һ�����е���ɫ��������������ɫʯ����Һ��죩��
���� ���⿼�����屽�����������ȡ������һ���ۺ��Խ�ǿ��ʵ���⣬�����Ʊ����ֲ�Ʒ�屽�������飬��Ҫ�������⼰װ��ͼʾ����ϵ��ѧ֪ʶ����������ɣ������Ѷ��еȣ�

 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�| A�� | 3 | B�� | ����3 | C�� | С��3 | D�� | ����ȷ�� |
| A�� | ��ҵ�Ϻϳɰ���ԭ�� | |
| B�� | ��ҵ�ϲ������� | |
| C�� | �ȵĴ�����Һϴ��Ч������ | |
| D�� | ����ʱ���Թܵײ���NH4Cl����ת�����Թ��϶� |
CO2��g��+H2��g��?CO��g��+H2O��g����H=Q kJ•mol-1
����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���£�
| t�� | 700 | 800 | 850 |
| K | 0.6 | 0.9 | 1.0 |
��������Ӧ��Q��0 ��ѡ�����������=������
���ں����£����жϸ÷�Ӧ�Ѵﵽ��ѧƽ��״̬��������cd��
a��������ѹǿ����
b���÷�Ӧ�ķ�Ӧ�ȡ�H����
c��H2�������������ٱ仯
d����λʱ��������H2O�����ʵ���������CO2�����ʵ������
��2��850��ʱ����2L���ܱ�������ͨ��1mol CO �� m mol H2O������Ӧ�ﵽƽ��ʱ��ƽ��������n��H2O��=2n��H2������m=2��
��3��850��ʱ����2L���ܱ�������ͨ��2mol CO �� 4mol H2O������Ӧ�ﵽƽ��ʱ��n ��H2��=$\frac{4}{3}$��
��4��850��ʱ����2L���ܱ�������ͨ��a mol CO��b mol H2O��c mol CO2��d molH2��
����Ҫ��Ӧ�ﵽƽ��ʱH2�����ʵ��������루3������ͬ����a��b��c��d֮��Ӧ����Ĺ�ϵ�ǣ���a+c������b+d��=1��2����c=d��
����Ҫ��Ӧ������H2�ķ�����У���a��b��c��d֮��Ӧ����Ĺ�ϵ�ǣ�ab��cd��
| A�� | ̼Ԫ�صĵ���ֻ���ڽ��ʯ��ʯī����ͬ�������� | |
| B�� | Mg��MgO��þԪ�����İ뾶��r��Mg2+����r��Mg�� | |
| C�� | �ֹ�$��_{����}^{Cl_{2}}$SiCl4$��_{����}^{H_{2}}$Si | |
| D�� | Mg��OH��2$\stackrel{����}{��}$MgCl2��aq��$\stackrel{���}{��}$Mg |
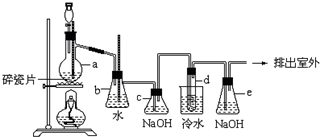 1��2-��������������Ϳ����������Ӽ���������������ɫҺ�壬�ܶ���2.18g/cm3���е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�������ͼ��ʾװ���Ʊ�1��2-�������飮���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Ũ��ˮ�����渲������ˮ����
1��2-��������������Ϳ����������Ӽ���������������ɫҺ�壬�ܶ���2.18g/cm3���е�131.4�棬�۵�9.79�棬������ˮ�������ڴ����ѡ���ͪ���л��ܼ�����ʵ���п�������ͼ��ʾװ���Ʊ�1��2-�������飮���з�Һ©������ƿa��װ���Ҵ���Ũ����Ļ��Һ���Թ�d��װ��Ũ��ˮ�����渲������ˮ����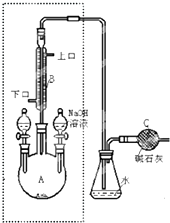 �Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺
�Ʊ��屽��ʵ��װ����ͼ��ʾ���ش��������⣺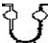 ������Ϊ��װ���п��Լ��뱽��CCl4Һ�壮
������Ϊ��װ���п��Լ��뱽��CCl4Һ�壮
 ��
��