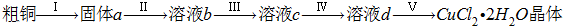��Ŀ����
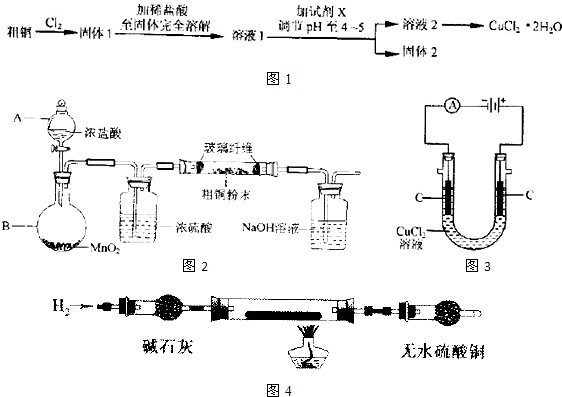
ij�о�С���ô�ͭ(������Fe)�����������Ʊ��Ȼ�ͭ����(CuCl2��2H2O)��
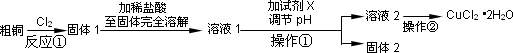
(1)ʵ���Ҳ�������ͼ��ʾ��װ�ã��ɽ���Ӧ�ٴ�ͭ��Cl2��Ӧת��Ϊ����1(���������ͼг�װ������ȥ)��
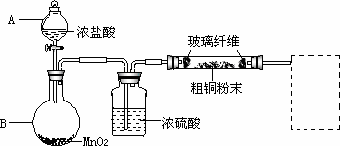
������A��������________��
�����Ӻ�װ�ú���ҩƷǰ��Ӧ�ý��е�ʵ�������________��
��װ��B�з�����Ӧ�����ӷ���ʽ��________��
����ͬѧ��ΪӦ��Ũ����ϴ��ƿǰ��������HCl��װ�ã�����Ϊ�Ƿ��Ҫ
(��ǡ���)________��
��������ȱ��ʵ��װ�ã����㻭��װ��ͼ������ҩƷ���ƣ�
(2)�Լ�X���ڵ���pH�Գ�ȥ���ʣ�X��ѡ�������Լ��е�(�����)________��
a��NaOH
b��NH3��H2O
c��CuO
d��Cu2(OH)2CO3
e��CuSO4
�����ٵ�������________��
(3)����Һ2ת��ΪCuCl2��2H2O�IJ��������У�������Һ��ɫ����ɫ��Ϊ��ɫ��С
��ͬѧ��̽����ԭ��
��֪�����Ȼ�ͭ��Һ��������ת����ϵ��
![]()
ȡ�Ȼ�ͭ�������Ƴ�����ɫ��ҺY����������ʵ�飬�����ܹ�֤��CuCl2��Һ��������ת����ϵ����(�����)________��
a����Yϡ�ͣ�������Һ����ɫ
b����Y�м���CuCl2���壬��Һ��Ϊ��ɫ
c����Y�м���NaCl���壬��Һ��Ϊ��ɫ
d��ȡY���е�⣬��Һ��ɫ������ʧ
(4)�����������Ȼ��������о�������Ũ����________�����ˡ�ϴ�ӡ����