题目内容
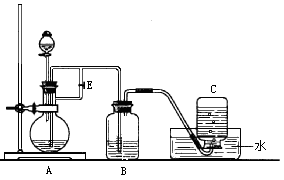
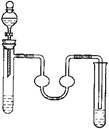
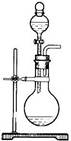
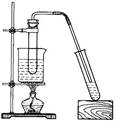
(共6分)实验室制取SO2的反应原理之一为:Na2SO3+H2SO4(浓)===Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:( ×100℅)
×100℅)
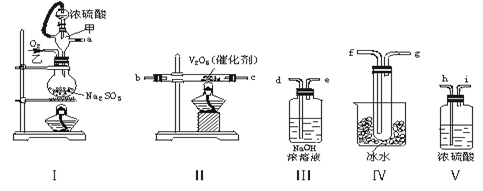
(1)这些装置的连接顺序(按气体左右的方向)是 → → → → → → → → (填各接口的编号)。
(2)实验时甲橡胶管的作用与原理是 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
(4)Ⅳ处观察到的现象是 。
(5)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为 。
 ×100℅)
×100℅)
(1)这些装置的连接顺序(按气体左右的方向)是 → → → → → → → → (填各接口的编号)。
(2)实验时甲橡胶管的作用与原理是 。
(3)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是 。
(4)Ⅳ处观察到的现象是 。
(5)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得Ⅲ处增重m g,则本实验中SO2的转化率为 。
(共6分)(1)a h i b c f g d?
(2)作用是使浓硫酸能顺利地滴入烧瓶中;原理是维持烧瓶内压强与分液漏斗内压强相等
(3)先加热V2O5,后缓缓滴入浓硫酸?
(4)有无色(或白色)晶体(或固体)生成
(5) ×100%或
×100%或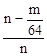 ×100%
×100%
(2)作用是使浓硫酸能顺利地滴入烧瓶中;原理是维持烧瓶内压强与分液漏斗内压强相等
(3)先加热V2O5,后缓缓滴入浓硫酸?
(4)有无色(或白色)晶体(或固体)生成
(5)
 ×100%或
×100%或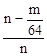 ×100%
×100%(1)装置I制取的SO2与O2经干燥后进入装置II,经过催化氧化后得到SO2、O2及生成的SO3的混合气体;为测定SO2与SO3的量,SO3在装置IV中经过冰水冷凝,而SO2将被随后的装置III中的碱液吸收;故接口的连接顺序为a h i b c f g d
(2)通过维持烧瓶内压强与分液漏斗内压强相等,使漏斗中的液体能顺利的滴下
(3)SO2的催化氧化是需要在高温下进行的,为提高SO2的转化率,应先加热装置II中的玻璃管,再滴加浓硫酸
(4)冰水的温度低于SO3的熔点,故在IV处可看到冷凝析出的SO3固体
(5)Ⅲ处增重m g即是部分转化后的SO2的质量,其物质的量为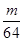 mol,而产生的SO2的总物质的量为n mol,故实验中SO2的转化率(2SO2+O2
mol,而产生的SO2的总物质的量为n mol,故实验中SO2的转化率(2SO2+O2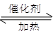 2SO3)为
2SO3)为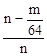 ×100%
×100%
(2)通过维持烧瓶内压强与分液漏斗内压强相等,使漏斗中的液体能顺利的滴下
(3)SO2的催化氧化是需要在高温下进行的,为提高SO2的转化率,应先加热装置II中的玻璃管,再滴加浓硫酸
(4)冰水的温度低于SO3的熔点,故在IV处可看到冷凝析出的SO3固体
(5)Ⅲ处增重m g即是部分转化后的SO2的质量,其物质的量为
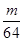 mol,而产生的SO2的总物质的量为n mol,故实验中SO2的转化率(2SO2+O2
mol,而产生的SO2的总物质的量为n mol,故实验中SO2的转化率(2SO2+O2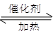 2SO3)为
2SO3)为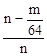 ×100%
×100%
练习册系列答案
相关题目
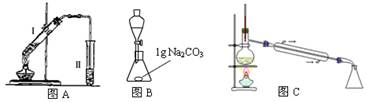
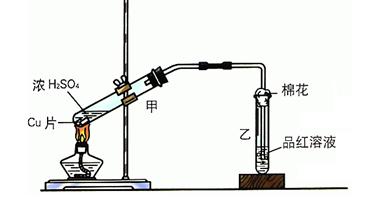
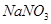 溶液,发现铜片溶解,此反应的离子方程式为 。
溶液,发现铜片溶解,此反应的离子方程式为 。