��Ŀ����
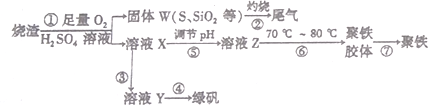
����Ŀ��ʵ�����������᳧����(��Ҫ�ɷ�Ϊ���������P����FeS��SiO2��)�Ʊ�����(��ʽ�������ľۺ���)���̷�(FeSO4��7H2O)����������£�
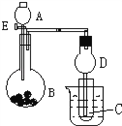
��1�����̢��У���Ҫ���������������____________________��
��2�����̢��в�����β����Դ��������Ⱦ����ѡ�������Լ��е�___________������
a.Ũ���� b.����ˮ c.NaOH��Һ d.Ũ����
��3�����̢�����FeS��O2��H2SO4��Ӧ�Ļ�ѧ����ʽΪ____________________��
��4�����̢ܵ�ʵ�������____________________��
��5�����̢���������ҺZ���ȵ�70����80����Ŀ���� ___________________��
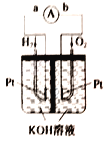
��6��ij���������������н���������������һ�����İ�����������Ӧ����������狀�����淋Ļ������Ϊ����Ʒ������������е�SO2��NO2�����ʵ���֮��Ϊ1��1����÷�Ӧ�Ļ�ѧ����ʽΪ__________________��
��7��ʵ����Ϊ�ⶨ���õ��ľ�����Ʒ����Ԫ�ص�������������������ʵ�顣���÷�����ƽ��ȡ��Ʒ2.700 g���ڽ���Ʒ����������������������Ȼ�����Һ���۹��ˡ�ϴ�ӡ�����������ù�������Ϊ3.495g�����þ�����Ҫ�ɷ�Ϊ[Fe(OH)SO4]a����þ�������Ԫ�ص���������Ϊ_________________��
���𰸡� ���� c 4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S ����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����� �ٽ�Fe3+��ˮ�����ɾ������� 4SO2+4NO2+12NH3+3O2+6H2O=4(NH3)2SO4+4NH4NO3 31.11%
����������1������ҺX�к���Fe2(SO4)3 ��H2SO4�����̷��������������塣���Թ��̢��У������������ǻ�ԭ��Fe�ۣ���1������W�к���S������ʱ�����SO2���塣SO2�����������ֱ���ŷŻ�Կ��������Ⱦ������Ũ���ᡢŨ���ᷴӦ����ˮ����Ч�����ã�������ǿ����Һ���գ���ѡc����3�����̢�����FeS��O2��H2SO4��Ӧ���������������ˮ����Ӧ�Ļ�ѧ����ʽΪ��4FeS+3O2+6H2SO4=2Fe2(SO4)3+6H2O+4S����4�����̢ܴ���ҺY�еõ��̷����壬ʵ������ǣ�����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ������5��Fe2(SO4)3��ǿ�������Σ�ˮ�����Fe(OH)3���塣�ε�ˮ�ⷴӦ�����ȷ�Ӧ���ڹ��̢��У�����ҺZ���ȵ�70һ80�棬Ŀ����Ϊ�˴ٽ�Fe3+��ˮ�����ɾ������壻��6�������е�SO2��NO2�����ʵ���֮��Ϊ1��1����һ�����İ�����������Ӧ����������狀�����泥���Ӧ�Ļ�ѧ����ʽΪ��4SO2+4NO2+12NH3+3O2+6H2O=4(NH3)2SO4+4NH4NO3����7���þ����ھ������ܽ����������Ȼ�����Һ���õ��ij���ΪBa SO4��n(Ba SO4)= ![]() =0.015mol������n(Fe)=0.015mol��m(Fe)=0.015mol��56g/mol=0.84g��������ھ�����FeԪ�صĺ���Ϊ
=0.015mol������n(Fe)=0.015mol��m(Fe)=0.015mol��56g/mol=0.84g��������ھ�����FeԪ�صĺ���Ϊ![]() ��100% =31.11%��
��100% =31.11%��

 ���ݼ���ϵ�д�
���ݼ���ϵ�д�����Ŀ������A��B��C��D���ֶ����ڷǽ���Ԫ�أ����ǵ�ԭ������������֮��Ϊ19�������ǵĻ������У���Ҫ���ϼ۾���ֹһ�֣�����һ����ͬ�Ļ��ϼۣ����ǵIJ����������£�
Ԫ�� | A | B | C | D |
ԭ�Ӱ뾶/nm | 0.102 | 0.077 | 0.117 | 0.075 |
��������ϼ� | ��4 | +4 |
��1��AԪ����Ԫ�����ڱ��е�λ��Ϊ ��
��2����DԪ�ص����ֳ������ۻ���������Ϸ�Ӧ������һ�����ӻ�����÷�Ӧ�Ļ�ѧ����ʽΪ ��
��3��B�ĵ�����D������������Ӧ��ˮ�����ڼ��������·�����Ӧ�Ļ�ѧ����ʽΪ ��
��4��C������Al����ijЩ�����ԣ���������ǿ�Ӧ��д��C������NaOH��Һ��Ӧ�Ļ�ѧ����ʽ�� ��
��5��A��B��C��D�����γɷ����к�18���ӵ��⻯���Щ�⻯��ķ���ʽ�ֱ�Ϊ ��