��Ŀ����
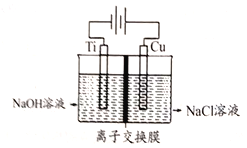
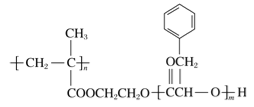
����Ŀ������ȼ�ϵ���Ƿ�����ɫ��ѧ��������ͷ���װ������ͼΪ���ʾ��ͼ���õ�ص缫����Ʋ㲬��(�����������������ǿ�������ȶ�)����ش��������⣺
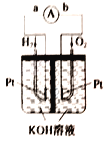
��1����װ������ת������Ҫ��ʽ��_________��
��2���ڵ����е�����������Ϊ_________(��a��b��ʾ)��
��3��������ӦʽΪ_________ ��
��4���缫����Ʋ��۵�Ŀ����_________��
��5�������õ���е�KOH��Һ��Ϊϡ���ᣬ�ڵ�·��Һ��H+��_________ (��������������������)�ƶ�����ع���ʱ�����ķ�ӦʽΪ_________��
���𰸡� �ɻ�ѧ��ת��Ϊ���� ��a��b H2��2OH����2e����2H2O ����缫��λ�������H2��O2���������ӿ�缫��Ӧ���� ���� O2��4H+��4e����2H2O
����������1��ԭ��ص�ʵ��Ϊ��ѧ��ת���ɵ��ܣ���2������ȼ�ϵ���ܷ�ӦΪ2H2+O2=2H2O������HԪ�صĻ��ϼ۴��������+1�ۣ�ʧȥ���ӣ������Ӵ�a����b����3������Ϊʧȥ���ӵ�һ������H2ʧ��������H����������Һ�Ǽ��Եģ�������ӦʽΪ H2��2OH����2e����2H2O����4���缫����Ʋ��۵�Ŀ��������缫��λ�������H2��O2���������ӿ�缫��Ӧ��������5�������õ���е�KOH��Һ��Ϊϡ���ᣬ�ڵ�·��Һ��H+����������ع���ʱ�����ķ�ӦʽΪO2��4H+��4e����2H2O��

 ��������ܸ�ϰϵ�д�
��������ܸ�ϰϵ�д�����Ŀ����1������P(s)��Cl2(g)������Ӧ����PCl3(g)��PCl5(g),��Ӧ�������¡�
2P(s)+3Cl2(g)=2PCl3(g) ��H=-612kJ/mol
2P(s)+5Cl2(g)=2PCl5(g) ��H=-798kJ/mol
��̬PCl5������̬PCl3��Cl2���Ȼ�ѧ����ʽΪ________.
��2����ͬ�¶��·�ӦCO(g)+H2O(g)![]() CO2(g)+H2(g) ��H1��ƽ�ⳣ�����±���ʾ��
CO2(g)+H2(g) ��H1��ƽ�ⳣ�����±���ʾ��
�¶�/�� | 400 | 500 | 800 |
ƽ�ⳣ��K | 9.94 | 9 | 1 |
����H1______0(����<����>��)����500��ʱ���ѵ����ʵ���Ũ�ȵ�CO��H2O(g)���뷴Ӧ�������ﵽƽ��ʱc(CO)=0.005mol/L��c(H2)=0.015mol/L,��CO��ƽ��ת����Ϊ______��
��3����һ������ľ����ܱ������У����ڷ�Ӧ2SO2(g)+O2(g)![]() 2SO3(g) ��H<0,�жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��_____________��
2SO3(g) ��H<0,�жϸ÷�Ӧ�ﵽƽ��״̬�ı�־��_____________��
A.SO2��SO3Ũ�����
B.�����л��������ܶȱ��ֲ���
C.������������¶ȱ��ֲ���
D.SO3������������SO2�������������
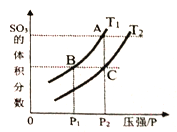
���¶�ΪT1��T2ʱ��ƽ����ϵSO3�����������ѹǿ�仯��������ͼ��ʾ����T1____T2 (����>������<")��������_____�������ӿ�����Ӧ�����ʣ����˸ı��¶ȣ���������_______������