题目内容
【题目】工业上设计用CO2来生产燃料甲醇,既减少二氧化碳气体,又得到宝贵的能源物质.为了探究反应原理,现进行如下实验:在体积为1L的密闭容器中,充入1molCO2和3molH2 , 某温度下发生反应:CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.0KJ/mol.测得CO2和CH3OH(g)的浓度随时间变化如图所示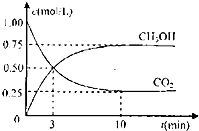
(1)该反应该温度下,化学平衡常数的值为
(2)下列说法中能作为反应达到平衡状态标志的是(填字母).
A.容器内压强不再发生变化
B.平均相对分子质量不再变化
C.c(CO2)和c(H2)之比等于1:3
D.相同时间内每断裂3molH﹣H键,同时断裂3molO﹣H键
(3)下列措施中能使 ![]() 减小的是
减小的是
A.再充入1molCO2和3molH2
B.将H2O(g)从体系中分离
C.充入He(g),使体系压强增大
D.升高温度.
【答案】
(1)5.33
(2)A,B,D
(3)D
【解析】解:(1.)图象中得到平衡状态二氧化碳浓度为0.25mol/L,甲醇浓度为0.75mol/L,利用化学平衡三行计算方法得到,
CO2(g)+3H2(g)CH3OH(g)+H2O(g),
开始(mol/L): 1 3 0 0
变化(mol/L): 0.75 2.25 0.75 0.75
平衡(mol/L): 0.25 0.75 0.75 0.75
平衡常数等于生成物的浓度幂之积除以反应物的浓度幂之积,则K= ![]() =
= ![]() =5.33,
=5.33,
所以答案是:5.33;
(2.)CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=﹣49.0KJ/mol,反应是气体体积减小的放热反应,
A.反应前后气体物质的量变化,当容器内压强不再发生变化,说明反应达到平衡状态,故A正确;
B.反应前后气体物质的量变化,气体质量不变,若平均相对分子质量不再变化,说明反应达到平衡状态,故B正确;
C.c(CO2)和c(H2)之比等于1:3是反应之比,不能说明正逆反应速率相同,故C错误;
D.生成物中H﹣O键不是一种物质中的化学键,甲醇和水分子中H﹣O键一定是1:2,依据化学方程式可知相同时间内每断裂3molH﹣H键,同时断裂3molO﹣H键,能说明正逆反应速率相同,故D正确;
故选ABD.
(3.)要使 ![]() 减小,应使平衡向逆反应方向移动,
减小,应使平衡向逆反应方向移动,
A.再充入1mol CO2和3mol H2 , 增大反应物浓度,平衡向正反应方向移动,则比值增大,故A错误;
B.将H2O(g)从体系中分离,平衡向正反应方向移动,比值增大,故B错误;
C.充入He(g),使体系压强增大,但对反应物质来说,浓度没有变化,平衡不移动,比值不变,故C错误;
D.因正反应放热,升高温度平衡向逆反应方向移动,则比值减小,故D正确;
所以答案是:D;
【考点精析】利用化学平衡状态本质及特征和化学平衡状态的判断对题目进行判断即可得到答案,需要熟知化学平衡状态的特征:“等”即 V正=V逆>0;“动”即是动态平衡,平衡时反应仍在进行;“定”即反应混合物中各组分百分含量不变;“变”即条件改变,平衡被打破,并在新的条件下建立新的化学平衡;与途径无关,外界条件不变,可逆反应无论是从正反应开始,还是从逆反应开始,都可建立同一平衡状态(等效);状态判断:①v(B耗)=v(B生)②v(C耗):v(D生)=x : y③c(C)、C%、n(C)%等不变④若A、B、C、D为气体,且m+n≠x+y,压强恒定⑤体系颜色不变⑥单位时间内某物质内化学键的断裂量等于形成量⑦体系平均式量恒定(m+n ≠ x+y)等.

 阅读快车系列答案
阅读快车系列答案