题目内容
【题目】向20 mL 0.5 mol·L-1硫酸溶液中逐滴加入烧碱溶液,测定混合溶液的温度变化如图所示。下列关于混合溶液的说法错误的是
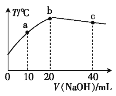
A. b点之前温度升高是因为发生了放热反应
B. bc段温度降低是因为与外界发生了热交换
C. c(NaOH)=0.5 mol·L-1
D. b点时酸碱恰好反应完全
【答案】C
【解析】
酸碱反应是放热反应,温度最高点(b)是酸碱恰好完全反应的点。
A.由分析可知,温度最高点(b)是酸碱恰好完全反应的点,b点之前发生酸碱中和反应,是放热反应,温度升高,故A正确;
B. 由分析可知,温度最高点(b)是酸碱恰好完全反应的点,bc段温度降低是因为与外界发生了热交换,故B正确;
C.由化学方程式H2SO4+ 2NaOH=Na2SO4+2H2O且b点时酸碱恰好反应完全可知,n(NaOH)=2n(H2SO4),即c(NaOH)V(NaOH)= 2c(H2SO4)V(H2SO4),代入数据计算c(NaOH)=![]() =1 mol·L-1,故C正确;
=1 mol·L-1,故C正确;
D. 温度最高点(b)是酸碱恰好完全反应的点,故D正确;
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目