��Ŀ����
����Ŀ����ҵ�Ϻϳɰ���ӦΪ��N2+3H2![]() 2NH3���ش��������⣺
2NH3���ش��������⣺
��1����Ӧ�����вĻ�ѧ����_______��
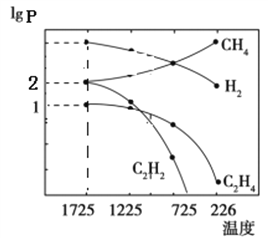
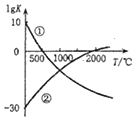
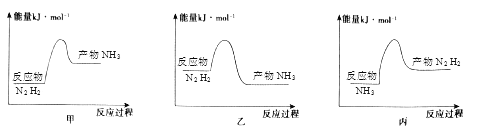
��2����Ӧ���ȣ��Ӽۼ��Ƕȷ�������Ӧ���ȵ�ԭ����_______������ͼ����ȷ����_______��
��3���������2L���ܱ������п�ʼ����1molN2��3molH2����Ӧ����Ũ���У����ʵ�Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
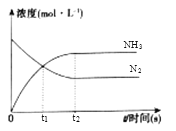
��t1ʱ����NH3�����ʵ�����_______����H2��ʾ�Ļ�ѧ��Ӧ���ʦԣ�H2��=_______��
�����и����ܱ�����Ӧ�ﵽ��ѧƽ��״̬����_______��
A.������������ܶȱ��ֲ���
B.�����������ѹǿ����
C.�����������
D.��3molH��H��ͬʱ�γ�6molN��H��
��4�����д�ʩ������ߺϳɰ���Ӧ��ѧ��Ӧ���ʵ���_______��
A.ʹ�ø�Ч���� B.���º����ٳ������� C.���ͷ�Ӧ�¶� D.�����������
���𰸡�N��N����HһH����Ӧ���еĻ�ѧ�����յ�����С���γɻ�ѧ���ų��������ҡ���2/3mol![]() mol��L-1��s-1B��CA��B
mol��L-1��s-1B��CA��B
��������
��1����Ӧ�����в��Ƿ�Ӧ���еĻ�ѧ����
��2����Ӧ���ȵ�ԭ���ǣ���Ӧ���еĻ�ѧ�����յ�����С���γ��������л�ѧ���ͷŵ����������ȷ�Ӧ��Ӧ����������������������������
��3����������ʽ���t1ʱNH3��N2��Ũ����ȣ�����t1ʱ����NH3���ʵ������û�ѧ��Ӧ���ʵĹ�ʽ�����ԣ�H2����
�����ݻ�ѧƽ��ı��ʱ�־���ﵽ��ѧƽ��ʱ����=����![]() 0����������־���ﵽ��ѧƽ��ʱ����ֵ�Ũ�ȱ��ֲ���������
0����������־���ﵽ��ѧƽ��ʱ����ֵ�Ũ�ȱ��ֲ���������
��4��������������Ի�ѧ��Ӧ���ʵ�Ӱ���������
��1����Ӧ�����в��Ƿ�Ӧ���еĻ�ѧ�����ϳɰ��ķ�Ӧ�з�Ӧ��ΪN2��H2��N2�ĽṹʽΪN![]() N��H2�ĽṹʽΪH��H����Ӧ�����вĻ�ѧ����N
N��H2�ĽṹʽΪH��H����Ӧ�����вĻ�ѧ����N![]() N����H��H����
N����H��H����
��2����Ӧ���ȵ�ԭ���ǣ���Ӧ���еĻ�ѧ�����յ�����С���γ��������л�ѧ���ͷŵ�������N2��H2�ϳ�NH3�ķ�ӦΪ���ȷ�Ӧ�����ȷ�Ӧ��Ӧ����������������������������N2��H2������������NH3����������NH3�ֽ��N2��H2�ķ�ӦΪ���ȷ�Ӧ����ȷ��ͼ������������
��3������0~t1��ת��N2���ʵ���Ũ��Ϊxmol/L��������ʽ
N2+3H2![]() 2NH3
2NH3
c����ʼ����mol/L�� 0.5 1.5 0
c��ת������mol/L�� x 3x 2x
c��t1ĩ����mol/L��0.5-x 1.5-3x 2x
����ͼ��t1ʱNH3��N2��Ũ����ȣ���0.5-x=2x�����x=![]() ��t1ʱ����NH3���ʵ���Ϊ2xmol/L
��t1ʱ����NH3���ʵ���Ϊ2xmol/L![]() 2L=2
2L=2![]() 2mol=
2mol=![]() mol����H2��ʾ�Ļ�ѧ��Ӧ�����ԣ�H2��=
mol����H2��ʾ�Ļ�ѧ��Ӧ�����ԣ�H2��=![]() =
=![]() =
=![]() mol/��L��s����
mol/��L��s����
��A����������غ㶨�ɣ���������������ʼ�ղ��䣬�������ݻ����䣬���������ܶ�ʼ�ղ��䣬������������ܶȱ��ֲ��䲻��˵����Ӧ�ﵽƽ��״̬��B��÷�Ӧ������Ӧ�����������С������ƽ�����������������ʵ�����С�����º��������У������ѹǿ��С���ﵽƽ��ʱ����������ʵ������䣬�����ѹǿ���䣬�����������ѹǿ������˵����Ӧ�ﵽƽ��״̬��C������ĺ���������˵����Ӧ�ﵽƽ��״̬��D���3molH��H��ͬʱ�γ�6molN��H��ֻ��������Ӧ������˵����Ӧ�ﵽƽ��״̬���ܱ�����Ӧ�ﵽƽ��״̬����BC����ѡBC��
��4��A�ʹ�ø�Ч�����ܼӿ�ϳɰ��Ļ�ѧ��Ӧ���ʣ�B����º����ٳ�������������Ӧ��H2��Ũ���ܼӿ�ϳɰ��Ļ�ѧ��Ӧ���ʣ�C����ͷ�Ӧ�¶ȣ������ϳɰ��Ļ�ѧ��Ӧ���ʣ�D������������������С�����ʵ�Ũ�ȣ��ϳɰ��Ļ�ѧ��Ӧ���ʼ���������ߺϳɰ���ѧ��Ӧ���ʵ���AB����ѡAB��

����Ŀ��������Ԫ��A��B��C��D��E�����ڱ��е�λ����ͼ��ʾ��A��B��C��Dλ���������ĸ����壬D��E������������20��
D | |||
A | B | C | E |
�ش��������⣺
��1��CԪ�������ڱ��е�λ����_______��EԪ�ص�������_______��
��2��AԪ������Ԫ���γɵ�ԭ�Ӹ�������1:1�Ļ�����Ļ�ѧʽ��_______���û����ﺬ�еĻ�ѧ��������_______��
��3��Bԭ�ӽṹʾ��ͼ��_______����ԭ�ӽṹ�Ƕȷ�����B��C�����Դ��ԭ����_______��
��4��Ԫ��D��Ԫ��E�ķǽ�����ǿ��������_______���û�ѧ����ʽ��ʾ����
��5��A��B��C��D���Ӱ뾶�ɴ�С��˳����_________����д���ӷ��ţ���
��6����B��C�ĵ���ѹ�ɱ�Ƭ�õ������Ӻ����ϡ�����У�������Ҫת����ʽ��_________��������Ӧʽ��_________��