题目内容
7.“龙珠天桥飞跨南与北”是平潮中学特色之一,下图是物质间转化关系构造的天桥.已知:A是一种无色无味气体;B、C、D、E、F的焰色均为黄色;物质D是发酵粉的主要成分,通常也用于治疗胃酸过多.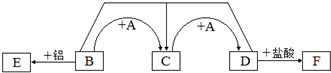
(1)A、D的化学式为CO2,NaHCO3;
(2)B与铝反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,取1mol铝与足量的B充分反应,转移电子数为3mol;
(3)E在一定条件下可转化为Al(OH)3胶体,用于吸附水中的悬浮泥沙并沉降下来,使水澄清.可利用丁达尔效应来区分胶体和溶液.
(4)胃舒平[主要成分为Al(OH)3]也是一种治疗胃酸过多的药,写出胃舒平与胃酸反应的离子方程式Al(OH)3+3H+═Al3++3H2O.
分析 B、C、D、E、F的焰色均为黄色,则B、C、D、E、F含有钠元素,物质D是发酵粉的主要成分,通常也用于治疗胃酸过多,则D为NaHCO3,D与盐酸反应生成F,则F为NaCl,A是一种无色无味气体,根据转化关系,B与A两步反应生成C和D,且B与铝反应生成E,则B为NaOH,C为Na2CO3,A为CO2,E为NaAlO2,据此答题.
解答 解:B、C、D、E、F的焰色均为黄色,则B、C、D、E、F含有钠元素,物质D是发酵粉的主要成分,通常也用于治疗胃酸过多,则D为NaHCO3,D与盐酸反应生成F,则F为NaCl,A是一种无色无味气体,根据转化关系,B与A两步反应生成C和D,且B与铝反应生成E,则B为NaOH,C为Na2CO3,A为CO2,E为NaAlO2,
(1)根据上面的分析,A为CO2,D为NaHCO3;
故答案为:CO2;NaHCO3;
(2)B为NaOH,B与铝反应的化学方程式为 2Al+2NaOH+2H2O═2NaAlO2+3H2↑,取1mol铝与足量的B充分反应,转移电子数为3mol,
故答案为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑;3;
(3)可利用 丁达尔效应来区分胶体和溶液,
故答案为:丁达尔效应;
(4)胃舒平[主要成分为Al(OH)3]也是一种治疗胃酸过多的药,胃舒平与胃酸反应的离子方程式为Al(OH)3+3H+═Al3++3H2O,
故答案为:Al(OH)3+3H+═Al3++3H2O.
点评 本题为框图式无机推断题,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论,把握常见物质的性质即可解答,题目难度中等.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
18.下列有关胶体的性质说法中正确的是( )
| A. | 溶液澄清透明,胶体浑浊不透明 | |
| B. | 加热和搅拌不可能引起胶体聚沉 | |
| C. | 将一束强光通过淀粉溶液时,能产生丁达尔现象 | |
| D. | 大气中PM2.5(直径≤2.5×10-6m的可吸入颗粒),一定属于胶体 |
12.用NA表示阿伏加德罗常数的值.下列说法中,正确的是( )
| A. | 1 mol OH-中含有的电子数目为9 NA | |
| B. | 标准状况下,22.4 L乙醇含有的分子数目为 NA | |
| C. | 1 L 0.1 mol/L NH4Cl溶液中,NH4+的数目为0.1 NA | |
| D. | 0.3 mol NO2溶于水生成HNO3,转移的电子数目为0.2 NA |
19.完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳气体,消耗掉8mol/L的氢氧化钠溶液50mL,则1mol无水乙醇的燃烧放出的热量不可能是( )
| A. | 10Q | B. | 5Q~10Q | C. | 3Q | D. | 8Q |
17.一定温度下将0.2mol气体A充入10L恒容密闭容器中,进行反应:2A(g)+B(g)?2C(g)+D(s)△H<0,一段时间后达到平衡,此反应过程中测定的数据如表所示,则下列说法正确的是( )
| t/min | 2 | 4 | 6 | 8 | 10 |
| n(A)/mol | 0.16 | 0.13 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2 min的平均速率ν(C)=0.02 mol•L-1•min-1 | |
| B. | 平衡后降低温度,反应达到新平衡前ν(逆)>ν(正) | |
| C. | 其他条件不变,10 min后再充入一定量的A,平衡正向移动,A的转化率变小 | |
| D. | 保持其他条件不变,反应在恒压下进行,平衡时A的体积分数与恒容条件下反应相同 |




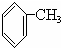 ; B
; B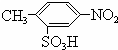 ;
;