题目内容
【题目】周期表中前四周期的元素A、Z、Q、R、T的原子序数依次增大,且A、Z、Q同周期。A共有两个原子轨道上有电子,且电子数目相同。Z、Q相邻,且Z中的未成对电子数为3个,R元素在地壳中含量位于金属元素的第二位。T是人类最早使用的元素,并以这种元素命名了我国的一个时代。请回答下面的问题:
(1)A、Z、Q第一电离能从小到大的顺序为:_______________(填元素符号),T的价层电子排布图为:__________________________。
(2)Q的基态原子中能量最高的电子,其电子云在空间有___________个方向,原子轨道呈_______形。
(3)Z3-的立体构型为____________,写出与Z3-互为等电子体的一种非极性分子化学式____________。
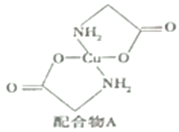
(4)在不同的温度下,A以ACl2和二聚体A2Cl4两种形式存在,二聚体的结构式如图所示:

①ACl2中A的杂化方式为______________________。
②1mol A2Cl4中含配位键的数目为____________。
(5)R单质的晶体在不同温度下有两种堆积方式,晶胞分别如图所示。体心立方晶胞和面心立方晶胞的棱边长分别为acm、bcm,则R单质的体心立方晶胞和面心立方晶胞的密度之比为_________,R原子配位数之比为_____________。

【答案】 Be<O<N ![]() 3 哑铃形 直线形 CO2(CS2等) sp 1.204×1024或2NA b3∶2a3 2∶3
3 哑铃形 直线形 CO2(CS2等) sp 1.204×1024或2NA b3∶2a3 2∶3
【解析】周期表中前四周期的元素A、Z、Q、R、T的原子序数依次增大,且A、Z、Q同周期。A共有两个原子轨道上有电子,且电子数目相同。A为Be元素;Z、Q相邻,且Z中的未成对电子数为3个,Z为N元素,Q为O元素;R元素在地壳中含量位于金属元素的第二位,R为Fe元素;T是人类最早使用的元素,并以这种元素命名了我国的一个时代,T为Cu元素。
(1) 同一周期,从左到右,第一电离能逐渐增大,但N的2p为半充满状态,较为稳定,A、Z、Q第一电离能从小到大的顺序为Be<O<N,铜为29号元素,价层电子排布图为![]() ,故答案为:Be<O<N;
,故答案为:Be<O<N;![]() ;
;
(2)Q为O元素,Q的基态原子中能量最高的电子为2p电子,其电子云在空间有x、y、z3个方向,原子轨道呈哑铃形,故答案为:3;哑铃形;
(3)N3-的价层电子对数=2+![]() ×(5+1-2×3)=2,立体构型为直线形,与N3-互为等电子体的一种非极性分子为CO2或CS2等,故答案为:直线形;CO2(或CS2等);
×(5+1-2×3)=2,立体构型为直线形,与N3-互为等电子体的一种非极性分子为CO2或CS2等,故答案为:直线形;CO2(或CS2等);
(4)在不同的温度下,Be以BeCl2和二聚体Be2Cl4两种形式存在。
①BeCl2中Be的价层电子对数=2+![]() ×(2-2×1)=2,采用sp杂化,故答案为:sp;
×(2-2×1)=2,采用sp杂化,故答案为:sp;
② 中的配位键为
中的配位键为 ,因此1mol Be2Cl4中含配位键的数目为1.204×1024,故答案为:1.204×1024;
,因此1mol Be2Cl4中含配位键的数目为1.204×1024,故答案为:1.204×1024;
(5)体心立方晶胞中含有的铁原子数目=8×![]() +1=2,面心立方晶胞中含有的铁原子数目=8×
+1=2,面心立方晶胞中含有的铁原子数目=8×![]() +6×
+6×![]() =4,则体心立方晶胞和面心立方晶胞的密度之比=
=4,则体心立方晶胞和面心立方晶胞的密度之比=![]() :
: ![]() =
=![]() ;体心立方晶胞中铁原子的配位数=8,面心立方晶胞中铁原子的配位数=12,铁原子配位数之比=
;体心立方晶胞中铁原子的配位数=8,面心立方晶胞中铁原子的配位数=12,铁原子配位数之比=![]() =
=![]() ,故答案为:
,故答案为: ![]() ;
; ![]() 。
。

【题目】阅读、分析下列两个材料:
材料一、
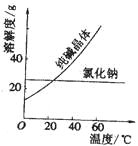
材料二、
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法 | B.萃取法 | C.“溶解、结晶、过滤”的方法 | D.分液法 |
(1) 将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用__________。
(2)将乙二醇和丙三醇相互分离的最佳方法是__________。