题目内容
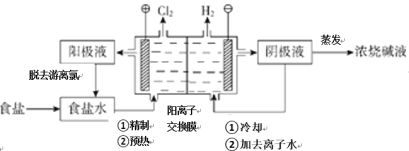
【题目】凯氏定氮法是测定蛋白质中氮含量的经典方法,其原理是用浓硫酸在催化剂存在下将样品中有机氮转化成铵盐,利用如图所示装置处理铵盐,然后通过滴定测量。已知:NH3+H3BO3=NH3·H3BO3;NH3·H3BO3+HCl= NH4Cl+ H3BO3。

回答下列问题:
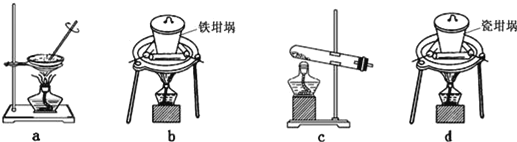
(1)a的作用是_______________。
(2)b中放入少量碎瓷片的目的是____________。f的名称是__________________。
(3)清洗仪器:g中加蒸馏水;打开k1,关闭k2、k3,加热b,蒸气充满管路;停止加热,关闭k1,g 中蒸馏水倒吸进入c,原因是____________;打开k2放掉水,重复操作2~3次。
(4)仪器清洗后,g中加入硼酸(H3BO3)和指示剂。铵盐试样由d注入e,随后注入氢氧化钠溶液,用蒸馏水冲洗d,关闭k3,d中保留少量水。打开k1,加热b,使水蒸气进入e。
①d中保留少量水的目的是___________________。
②e中主要反应的离子方程式为________________,e采用中空双层玻璃瓶的作用是________。
(5)取某甘氨酸(C2H5NO2)样品m 克进行测定,滴定g中吸收液时消耗浓度为c mol·L–1的盐酸V mL,则样品中氮的质量分数为_________%,样品的纯度≤_______%。
【答案】避免b中压强过大 防止暴沸 直形冷凝管 c中温度下降,管路中形成负压 液封,防止氨气逸出 ![]() +OH
+OH![]() NH3↑+H2O 保温使氨完全蒸出
NH3↑+H2O 保温使氨完全蒸出 ![]()
![]()
【解析】
a与大气相通,其作用是平衡气压,使b中气压与大气压相等,以避免b中压强过大导致容器炸裂;b中的液体为蒸馏水,一般纯液体在加热过程中容易引起暴沸,所以需要加入碎瓷片来防止暴沸;体系内充满水蒸气后,关闭k1,水蒸气会慢慢冷凝为水,体系内气压小于外界大气压,在大气压的作用下,锥形瓶内的蒸馏水被倒吸入e中,e中的水再倒吸入c中;氨气的密度比空气的小,若d留有缝隙,易导致氨气泄露出去,所以d中保留少量水的目的是液封,防止氨气逸出;e装置是用来制取氨气的,g装置是用来吸收氨气的,制取氨气时发生的反应为:![]() +OH
+OH![]() NH3↑+H2O;求样品中氮元素的质量分数时,根据反应NH2·HBO2+HCl= NH4Cl+H3BO2,可知n(N)=n(HCl),求出消耗的HCl的物质的量即可求出N的物质的量,根据甘氨酸的分子量及样品的质量,可求出样品的纯度,同时,根据其摩尔质量为14g/mol和样品的质量为m 克,可求出样品中的氮的质量分数。
NH3↑+H2O;求样品中氮元素的质量分数时,根据反应NH2·HBO2+HCl= NH4Cl+H3BO2,可知n(N)=n(HCl),求出消耗的HCl的物质的量即可求出N的物质的量,根据甘氨酸的分子量及样品的质量,可求出样品的纯度,同时,根据其摩尔质量为14g/mol和样品的质量为m 克,可求出样品中的氮的质量分数。
(1) a的作用是平衡气压,以避免b中压强过大;
(2) b中放入少量碎瓷片的目的是防止暴沸。f的名称是直形冷凝管;
(3) g中蒸馏水倒吸进入c的原因是g、e及其所连接的管道内水蒸气冷凝为水后,气压远小于外界大气压,在大气压的作用下,锥形瓶内的蒸馏水被倒吸入中;
(4)①d中保留少量水的目的是液封,防止氨气逸出;
②e中主要反应是铵盐与碱在加热条件下的反应,离子方程式为![]() +OH
+OH![]() NH3↑+H2O; e采用中空双层玻璃瓶的作用是保温减少热量损失,有利于铵根转化为氨气逸出;
NH3↑+H2O; e采用中空双层玻璃瓶的作用是保温减少热量损失,有利于铵根转化为氨气逸出;
(5)取某甘氨酸(C2H5NO2)样品m克进行测定,滴定g中吸收液时消耗浓度为c mol/L的盐酸VmL,根据反应NH2·HBO2+HCl= NH4Cl+H3BO2,可以求出样品中n (N)=n(HCl)=c mol/L×V×10-3 L=0.001cV mol, 则样品中氮的质量分数为(0.001cV×14g/mol)/ mg×100%= ![]() % ,样品中甘氨酸的质量≤0.001cV×75g,所以样品的纯度≤
% ,样品中甘氨酸的质量≤0.001cV×75g,所以样品的纯度≤![]() % 。
% 。