题目内容
20.已知一定温度和压强下,由H2和CO反应合成优质燃料甲醇:CO(g)+2H2(g)?CH3OH(g)△H=-91kJ/mo1①在相同条件下要想得到182kJ热量,加入各物质的物质的量可能是D.
A.2mo1CO和4molH2
B.2mo1CO、4molH2和1mol CH3OH(g)
C.4mo1CO和4molH2
D.4mo1CO和6molH2
②将1mol CO和2mol H2充入一密闭容器中,保持恒温恒压时进行反应,达到平衡时,测得CO的转化率为20%.若在相同条件下,起始时在该容器中充入1mol CH3OH(g),反应达到平衡时的热量变化是吸收(填“吸收”或“放出”)72.8kJ热量.
分析 ①由反应方程式可知生成1mol的CH3OH时放热91 kJ,想得到182kJ热量,则需生成2molCH3OH;由于反应是可逆反应,不可能完全进行到底,所以要得到2molCH3OH,CO与H2物质的量必须要多于2mol和4mol;
②已知反应:CO(g)+2H2(g)?CH3OH(g)△H=-91kJ/mo1,则有CH3OH(g)?CO(g)+2H2(g);△H=+91KJ•mol-1,保持恒温恒压,将1mol CO和2mol H2充入一密闭容器中与起始时在该容器中充入1mol CH3OH(g),为等效平衡状态,平衡时两种不同的途径平衡状态相同,各物质的含量、物质的量等都相同,以此计算.
解答 解:①由反应方程式可知生成1mol的CH3OH时放热91 kJ,想得到182kJ热量,则需生成2molCH3OH;由于反应是可逆反应,不可能完全进行到底,所以要得到2molCH3OH,CO与H2物质的量必须要多于2mol和4mol,
故答案为:D;
②CO(g)+2H2(g)?CH3OH(g)△H=-91kJ/mo1
起始量 1 2 0
转化量0.2 0.4 0.2
平衡量0.8 1.6 0.2
CH3OH(g)?CO(g)+2H2(g)△H=+91KJ•mol-1,
起始量 1 0 0
转化量 0.8 0.8 1.6
转化量 0.2 0.8 1.6
生成1molCH3OH放热91KJ,分解1molCH3OH吸热91KJ,分解0.8mol甲醇,吸热72.8KJ,
故答案为:吸收;72.8.
点评 本题考查了等效平衡的应用、逆反应的反应热,题目难度中等,抓住基础是关键.

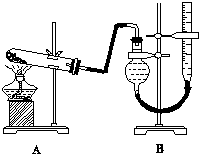 某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:
某实验小组欲制取氧化铜并证明氧化铜能加快氯酸钾的分解,进行了如下实验:(一)制取氧化铜
①称取2g CuSO4•5H2O研细后倒入烧杯,加10mL蒸馏水溶解;
②向上述CuSO4溶液中逐滴加入NaOH溶液,直到不再产生沉淀,然后将所得混合物转移到蒸发皿,加热至沉淀全部变为黑色;
③将步骤②所得混合物过滤、洗涤,晾干后研细备用.
回答下列问题:
(1)上述实验步骤中需要使用玻璃棒的是①②③(填实验序号),步骤①③中研磨固体所用仪器的名称是研钵;
(二)证明氧化铜能加快氯酸钾的分解并与二氧化锰的催化效果进行比较,相关数据如下:
| 实验序号 | KClO3质量 | 其他物质质量 | 待测数据 |
| ④ | 1.2g | 无其他物质 | |
| ⑤[ | 1.2g | CuO 0.5g | |
| ⑥ | 1.2g | MnO2 0.5g |
(2)上述实验中“待测数据”指产生25mL气体所需时间;
(3)本实验装置图中量气装置B由干燥管、乳胶管和50mL滴定管改造后组装而成,此处所用滴定管是碱式(选填“酸式”或“碱式”)滴定管;读数时需要注意①上下移动右管使两液面相平; ②视线与刻度线相平
(4)为探究CuO在实验⑤中是否起催化作用,需补做如下实验(无需写出具体操作):
a.检测CuO反应前后质量是否改变,
b.CuO的化学性质有没有改变.

| 选项 | a中的物质 | b中的物质 | c中的物质 | d中的物质 | d中的物质 |
| A | 浓硫酸 | 铜片 | 品红溶液 | 酸性高锰酸钾溶液 | c,d中溶液颜色均褪色,依次体现SO2漂白性和还原性 |
| B | 浓硫酸 | 蔗糖 | 紫色石蕊溶液 | NaOH溶液 | c中溶液变红色,不能判断是SO2的作用 |
| C | 稀硝酸 | Cu | 收集NO2 | H2O | d中反应每消耗3mol氧化剂,转移2mol电子 |
| D | 浓氨水 | 碱石灰 | 收集NH3 | 稀H2SO4 | d中反应产物可作肥料 |
| A. | A | B. | B | C. | C | D. | D |
| A. | Na+、MnO4-、K+、NO3-SO32- | B. | Na+、S2-、SO32-、H+、NO3- | ||
| C. | Na+、S2-、OH-、K+、Cl- | D. | HCO3-、H+、Na+、Ca2+ SO32- |
| A. | 电池工作时,锌失去电子 | |
| B. | 电池正极的电极反应式为:2MnO2+2H2O+2e-═2MnOOH+2OH- | |
| C. | 电池工作时,电子由正极通过外电路流向负极 | |
| D. | 外电路中每通过0.2mol 电子,锌的质量理论上减少6.5g |
| A. | 对于有气体参与的反应,增大压强,活化分子总数增多,化学反应速率增大 | |
| B. | 对放热反应而言,升高温度,活化分子百分数减少,化学反应速率减小 | |
| C. | 活化分子间发生的碰撞为有效碰撞 | |
| D. | 使用催化剂,活化分子百分数增多,化学反应速率增大 |
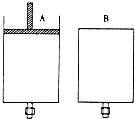 有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应:
有两只密闭容器A和B,A容器有一个移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两只容器中分别充入等量的体积比为2:1的SO2与O2的混合气体,并使A和B容积相等(如图).在保持400℃的条件下使之发生如下反应: