题目内容
20.以NA表示阿伏伽德罗常数,下列说法中正确的是( )| A. | 58.5 g氯化钠固体中含有NA个氯化钠分子 | |
| B. | 1mol Fe参与反应失去电子数目一定为2NA | |
| C. | 金属钠和氧气反应制取过氧化钠,每生成1mol过氧化钠,转移电子数为4NA | |
| D. | 常温下,46 g NO2和N2O4的混合物中含有的氮原子数为NA |
分析 A、氯化钠是离子化合物;
B、铁的价态有+2价和+3价;
C、生成1mol过氧化钠消耗2mol钠;
D、NO2和N2O4的最简式均为NO2.
解答 解:A、氯化钠是离子化合物,是由离子构成的,无氯化钠分子,故A错误;
B、铁的价态有+2价和+3价,故1mol铁参与反应失去的电子可能为2NA个,也可能为3NA个,故B错误;
C、生成1mol过氧化钠消耗2mol钠,而反应后钠元素变为+1价,而2mol钠失去2mol电子即2NA个,故反应转移2NA个电子,故C错误;
D、NO2和N2O4的最简式均为NO2,故46g混合物中含有的NO2的物质的量为n=$\frac{46g}{46g/mol}$=1mol,则含NA个氮原子,故D正确.
故选D.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
10.下列各项叙述中,正确的是( )
| A. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| B. | 24Cr原子的电子排布式是1s22s22p63s23p63d44s2 | |
| C. | 所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 | |
| D. | 价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
11.25℃和1.01×105Pa时,2N2O5(g)=4NO2(g)+O2(g)△H=+56.76kJ/mol,该反应能自发进行的原因是( )
| A. | 是吸热反应 | B. | 是放热反应 | C. | 是熵减少的反应 | D. | 是熵增大的反应 |
12.有A、B、C三种可溶性的盐,阴、阳离子各不相同,其阴离子的摩尔质量按A、B、C得顺序依次增大.将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子,同时生成一种白色沉淀AgCl,则A的化学式可能是( )
| A. | K2SO4 | B. | AgNO3 | C. | FeCl3 | D. | KCl |
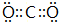 .
.