题目内容
【题目】测定稀硫酸和氢氧化钠溶液反应的中和热(实验装置如图所示)。
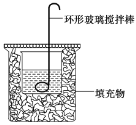
(1)图中尚缺少的一种仪器是________。
(2)实验时环形玻璃搅拌棒的运动方向是________。
a.上下运动 b.左右运动 c.顺时针运动 d.逆时针运动
(3)该同学每次分别取0.50mol·L-1 50mL NaOH溶液和0.50mol·L -1 30mL硫酸进行实验,通过多次实验测定中和热ΔH= -53.5kJ·mol-1,与57.3kJ·mol-1有偏差,产生偏差的原因不可能__(填字母)。
a.实验装置保温、隔热效果差
b.用量筒量取NaOH溶液的体积时仰视读数
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度
(4)在测定中和热的实验中,下列说法正确的是(____)
A.使用环形玻璃棒是为了加快反应速率,减小实验误差
B.为了准确测定反应混合溶液的温度,实验中温度计水银球应与小烧杯底部接触
C.用0.5mol·L-1 NaOH溶液分别与0.5mol·L-1的盐酸、醋酸溶液反应,如所取的溶液体积相等,则测得的中和热数值相同
D.在测定中和热实验中需要使用的仪器有天平、量筒、烧杯、滴定管、温度计
(5)用相同浓度和体积的氨水代替溶液进行上述实验,测得的中和热![]() H会____(填“偏大”、“偏小”或“无影响”)。
H会____(填“偏大”、“偏小”或“无影响”)。
【答案】温度计 a b A 偏大
【解析】
(1)测定反应的中和热,需要测定溶液温度;
(2)测定中和热需要烧杯内液体温度上下一致;
(3)53.5kJ·mol-1<57.3kJ·mol-1,说明实验过程中热量有损失;
(4)测定中和热实验尽可能防止热量损失;
(5)氨水是弱碱,电离吸热。
(1)测定稀硫酸和氢氧化钠溶液反应的中和热,需要测定溶液温度,缺少的一种仪器是温度计;
(2)测定中和热需要烧杯内液体温度上下一致,所以环形玻璃搅拌棒的运动方向是上下运动,故选a;
(3)a、装置保温、隔热效果差,热量损失大,测得的热量偏小,中和热的数值偏小, a错误;
b、用量筒量取NaOH溶液的体积时仰视读数,氢氧化钠的物质的量偏多,生成水偏多,放出的热量多,b正确;
c.分多次把NaOH溶液倒入盛有硫酸的小烧杯中,热量损失大,测得的热量偏小,中和热的数值偏小,c错误;
d.用温度计测定NaOH溶液起始温度后直接测定硫酸溶液的温度,硫酸溶液的起始温度偏高,测得的热量偏小,中和热的数值偏小,d错误;
故选b;
(4)A.使用环形玻璃棒是为了加快反应速率,使溶液内温度均一,减小实验误差,A正确;
B.测量溶液温度,温度计水银球应不能与小烧杯壁接触,B错误;
C.醋酸是弱酸,电离吸热,相同条件下,用NaOH溶液与醋酸溶液反应,测得的中和热数值偏小,C错误;
D.在测定中和热实验中需要使用的仪器有量筒、烧杯、温度计,用不到天平、滴定管,故错误;
故选A;
(5)氨水是弱碱,电离吸热,用相同浓度和体积的氨水代替溶液进行上述实验,测得的中和热ΔH会偏大。

 芝麻开花课程新体验系列答案
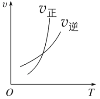
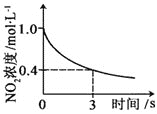
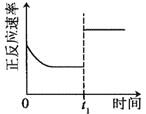
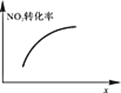
芝麻开花课程新体验系列答案【题目】臭氧是理想的烟气脱硝剂,其脱硝反应为:2NO2(g)+O3(g)![]() N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
N2O5(g)+O2(g),反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是()
A | B | C | D |
|
|
|
|
升高温度,正反应方向平衡常数减小 | 0~3s内,反应速率为:v(NO2)=0.2 mol·L-1·s-1 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
A. AB. BC. CD. D
【题目】亚硝酰氯(ClNO)是有机合成中的重要试剂,可通过反应:2NO(g)+Cl2(g)2ClNO(g)获得。
(1)氮氧化物与悬浮在大气中海盐粒子的相互作用时,涉及如下反应:
①2NO2(g)+NaCl(s)![]() NaNO3(s)+ClNO(g) K1
NaNO3(s)+ClNO(g) K1
②4NO2(g)+2NaCl(s)![]() 2NaNO3(s)+2NO(g)+Cl2(g) K2
2NaNO3(s)+2NO(g)+Cl2(g) K2
③2NO(g)+Cl2(g)![]() 2ClNO(g) K3
2ClNO(g) K3
则K3=__________(用K1、K2表示)。
(2)300℃时,2NO(g)+Cl2(g)2ClNO(g)的正反应速率表达式为v(正)=k·cn(ClNO),测得速率和浓度的关系如表所示:
序号 | c(ClNO)/(mol/L) | v/(x10-8mol·L-1·S-1) |
① | 0.30 | 0.36 |
② | 0.60 | 1.44 |
③ | 0.90 | 3.24 |
k=__________________________。
(3)按投料比[n(NO):n(Cl2)=2:1]把 NO和Cl2加入到一恒压的密闭容器中发生反应,平衡时NO的转化率与温度T、压强p(总压)的关系如图A所示:
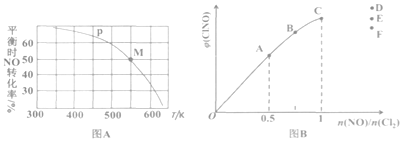
①在p压强条件下,M点时容器内NO的体积分数为______________。
②若反应一直保持在P压强条件下进行,则M点的分压平衡常数KP=________(用含P的表达式表示,用平衡分压代替平衡浓度计算,分压=总压 x体积分数)。
(4)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2)的变化图像如图B所示,则A、B、C三状态中,NO的转化率最大的是________点,当n(NO)/n(Cl2)=1.5时,达到平衡状态ClNO的体积分数可能是D、E、F三点中的_______点。
【题目】在Na+浓度为0.5mol·L-1的某澄清溶液中,还可能含有下表中的若干种离子。
阳离子 | K+ Ag+ Mg2+ Ba2+ |
阴离子 | NO3- CO32- Cl- SO42- |
现取该溶液100mL进行如下实验(气体体积均在标准状况下测定)。
序号 | 实验内容 | 实验结果 |
Ⅰ | 向该溶液中加入足量稀硝酸 | 放出标准状况下0.56L无色气体 |
Ⅱ | 向Ⅰ的反应混合液中加入过量的硝酸钡,产生白色沉淀,对沉淀洗涤、干燥,称量所得固体质量 | 固体质量为9.32克 |
Ⅲ | 向Ⅱ的滤液中滴加硝酸银溶液 | 无明显现象 |
请回答下列问题。
(1)实验Ⅰ能确定一定不存在的离子是___。
(2)实验Ⅰ中生成气体的离子方程式为___。
(3)通过实验Ⅰ、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定不存在的离子填“0”,不能确定是否存在的离子填“?”)。___
阴离子 | NO3- | CO32- | Cl- | SO42- |
c/mol·L-1 |
(4)判断K+是否存在,若存在求其最小浓度,若不存在说明理由:___。