题目内容
(1)用过量铜片与0.2 mol浓H2SO4共热足够长时间(只考虑铜与浓H2SO4反应,忽略其他副反应),甲认为产生的SO2少于0.1 mol,理由是________________________________________________________________________
________________________________________________________________________;
而乙同学认为产生的SO2为0.1 mol,理由是_____________________________________________。
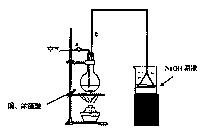
(2)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为___________________________________________________________。
利用铜制备CuSO4的另一种方法可用化学方程式表示为_________________________________________。
以上两种方法________(填“前”或“后”)者好,原因是_____________________。
________________________________________________________________________;
而乙同学认为产生的SO2为0.1 mol,理由是_____________________________________________。
(2)实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的。铜屑在此状态下被溶解的化学方程式为___________________________________________________________。
利用铜制备CuSO4的另一种方法可用化学方程式表示为_________________________________________。
以上两种方法________(填“前”或“后”)者好,原因是_____________________。
(1)由反应Cu+H2SO4(浓)CuSO4+SO2↑+2H2O知,当0.2 mol浓H2SO4全部反应时才生成0.1 mol SO2,随着反应进行,浓H2SO4变稀,不能与Cu反应,故甲认为少于0.1 mol SO2;乙同学认为稀H2SO4与铜反应由于加热时间足够长,水比H2SO4易挥发,因此,H2SO4始终保持较高浓度,直至与铜完全反应为止;(2)2Cu+2H2SO4(稀)+O22CuSO4+2H2O Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O'前'若制得1 mol CuSO4,第一种方法只需1 mol H2SO4,而第二种方法则要用2 mol H2SO4,而且生成的SO2会造成大气污染
(1)过量铜片与0.2 mol H2SO4(浓)反应,理论上生成0.1 mol SO2,但当浓H2SO4变稀时与Cu不反应,故甲认为少于0.1 mol SO2;乙同学认为加热足够长时间,水挥发后,稀H2SO4又变成浓H2SO4,直至与Cu反应完全。(2)两种方法前者好因为不产生有污染的SO2气体,且生成等量的CuSO4耗H2SO4少。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

 2NH3(g) △H = -92.4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。
2NH3(g) △H = -92.4 kJ·mol-1,一定条件下的密闭容器中,该反应达到平衡,要提高N2的转化率,可以采取的措施是__________(填字母代号)。

 。
。 硫酸
硫酸