��Ŀ����
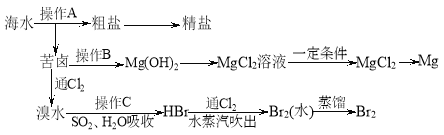
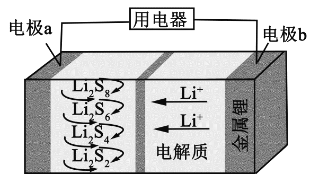
����Ŀ��ȫ��̬����������ܶȸߡ��ɱ���,�乤��ԭ����ͼ��ʾ,���е缫a���ò���ʯīϩ��S8����,��ط�ӦΪ��16Li+xS8=8Li2Sx(2x8).����˵���������( )
A. ��ع���ʱ,�����ɷ�����Ӧ��2Li2S6+2Li++2e=3Li2S4
B. ��س��ʱ��Խ��,����е�Li2S2��Խ��
C. ʯīϩ��������Ҫ����ߵ缫a�ĵ�����
D. ��ع���ʱ�����·������0.04mol���ӣ��������ϼ���0.28g
���𰸡�B
��������
A. ԭ��ع���ʱLi+ �������ƶ�������ͼʾ��֪������ԭ��Ӧ��2Li2S6+2Li++2e=3Li2S4����A����ȷ��
B. ��س��ʱ��LiSx�������ŵ磬S�Ļ��ϼ����ߣ�������Li2S2ת��ΪLi2S4��Li2S6��Li2S8���ʳ��ʱ��Խ����Li2S2����Խ�٣���B�����
C.ʯīϩ�ܹ����磬����������ߵ缫a�ĵ����ԣ���C����ȷ��
D. ���·������0.04mol����ʱ��������Li�����ģ�����Li�����ʵ���Ϊ0.04mol���������ϼ���Ϊ0.04��7=0.28g����D����ȷ��
��������������ѡB��

����Ŀ����֪��������ĵ���ƽ�ⳣ�����±���ʾ:
���� | ���� | ������ | ̼�� | ������ |
����ƽ�ⳣ��Ka(25��) | 1.75��10-5 | 2.98��10-8 | Ka1=4.3��10-7 Ka2=5.61��10-11 | Ka1=1.54��10-7 Ka2=1.02��10-7 |
�������ӷ���ʽ��ȷ����
A. ������CO2ͨ��NaClO��Һ��:CO2+H2O+2C1O-==CO32-+2HClO
B. ������SO2ͨ��Na2CO3��Һ��:SO2+H2O+2CO32-==SO32-+2HCO3-
C. ������SO2ͨ��Ca(ClO)2��Һ��:SO2+H2O+Ca2++2ClO-==CaSO3��+2HClO
D. ��ͬŨ�ȵ�NaHCO3��Һ��NaHSO3��Һ��������:H++HCO3-==CO2��+H2O