题目内容
【题目】乙二醇是工业常见的有机原料,常用来制取纺织工业的乙二醛和化妆品行业的乙醛酸。
①乙二醇(HOCH2CH2OH)气相催化氧化法制取乙二醛(OHC-CHO),主要反应为:HOCH2CH2OH(g)+O2(g)![]() OHC—CHO(g)+2H2O(g) H
OHC—CHO(g)+2H2O(g) H
化学键 | O—H | C—H | C—O | C=O | O=O | C—C |
键能(kJ·mol-1) | 436 | 413 | 356 | 745 | 493 | 346 |
则H=_____kJ·mol-1。
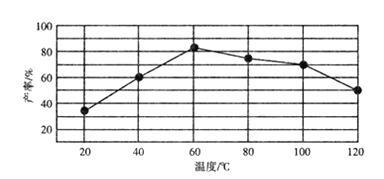
②当原料气中氧醇比(氧气和乙二醇的物质的量之比)一定时,乙二醛和副产物CO2的产率与反应温度的关系如图所示,则反应中应控制的适宜温度是___(填字母)。
a.低于450℃
b.450℃~490℃
c.高于495℃
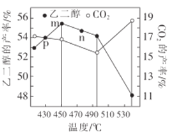
p、m、n三点中____是平衡点,__是逆反应速率最快的点。
③温度超过495℃时,乙二醛的产率直线下降的原因是___。
(2)将乙二醇氧化为乙二酸,再利用乙二酸(HOOCCOOH)通过电解制备乙醛酸,阴极的电极反应式为____。
(3)液相氧化制备乙醛酸是近年研究的热点。向25L某浓度的乙二醛溶液中,加入适量的催化剂V2O5/C,以0.1mol·L-1的流速通入氧气,测得溶液中乙二醛的浓度、溶液的pH随时间变化的关系如图所示:
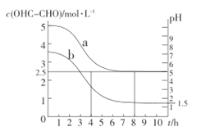
①图中曲线___(填“a”或“b”)表示溶液的pH值随时间变化的曲线。
②V2O5/C表示将催化剂覆盖在纳米碳纤维上,其目的是___。
③写出制备乙醛酸(HOC—COOH)的化学反应方程式:____,根据图中数据算出8h内乙醛酸的平均生成速率v(HOC—COOH)=____;该实验条件下乙醛酸的电离常数Ka=___。
【答案】-331 b m、n n 温度过高,乙二醇被大量转化为CO2 HOOCCOOH+2H++2e-=OHCCOOH+H2O b 增大接触面积,加快反应速率 2OHC—CHO+O2![]() 2OHC—COOH 0.3125mol·L-1·h-1 4×10-4
2OHC—COOH 0.3125mol·L-1·h-1 4×10-4
【解析】
(1)①根据△H=反应物键能总和-生成物键能总和计算;②反应中应控制的适宜温度是此温度下,乙二醛产率高,CO2的产率要低;HOCH2CH2OH(g)+O2(g)OHC-CHO(g)+2H2O(g)该反应为放热反应,m点之前反应未达到平衡,m达到平衡,升高温度,平衡逆向移动;③由图可知,温度超过495℃时,乙二醛的产率直线下降,而CO2的产率直线上升,据此分析解答;
(2)HOOCCOOH与OHC-COOH对比,可知HOOCCOOH比OHC-COOH多一个O,发生还原反应,而阴极发生还原反应,生成OHC-COOH和H2O,据此书写电极反应式;
(3)①乙二醛溶液显中性,即起始溶液pH为7,根据图分析判断;②将催化剂覆盖在纳米碳纤维上,可以增大接触面积;③乙二醛(OHC-CHO)与氧气反应生成乙醛酸(HOC-COOH)根据守恒原则结合图象书写化学方程式;由图可知,乙二醛起始浓度为5mol/L,8h后其浓度为2.5mol/L,则△c(OHC-CHO)=2.5mol/L,根据方程式得出△c(HOC-COOH),结合v=![]() 计算8h内乙醛酸的平均生成速率v(HOC-COOH);根据HOC-COOH的浓度为2.5mol/L时pH=1.5,结合电离方程式HOC-COOHHOC-COO-+H+计算。
计算8h内乙醛酸的平均生成速率v(HOC-COOH);根据HOC-COOH的浓度为2.5mol/L时pH=1.5,结合电离方程式HOC-COOHHOC-COO-+H+计算。
(1)①HOCH2CH2OH(g)+O2(g)![]() OHC—CHO(g)+2H2O(g) 反应物含有4个
OHC—CHO(g)+2H2O(g) 反应物含有4个![]() ,2个
,2个![]() ,2个
,2个![]() ,1个
,1个![]() ,1个
,1个![]() ;生成物含有2个
;生成物含有2个![]() ,2个
,2个![]() ,4个
,4个![]() ,1个
,1个![]() ,△H=反应物键能总和-生成物键能总和=[436×2+346+413×4+2×356+493-(423×2+346+745×2+2××2436)]kJmol-1=-331kJmol-1,故答案为:-331;
,△H=反应物键能总和-生成物键能总和=[436×2+346+413×4+2×356+493-(423×2+346+745×2+2××2436)]kJmol-1=-331kJmol-1,故答案为:-331;
②反应中应控制的适宜温度是此温度下,乙二醛产率高,CO2的产率要低,则450°C~490°C为最适宜温度;HOCH2CH2OH(g)+O2(g)OHC-CHO(g)+2H2O(g)△H= -331kJmol-1,该反应为放热反应,m点之前反应未达到平衡,m点达到平衡,升高温度,平衡逆向移动,故m、n点是平衡点;温度越高,反应速率越快,则n点速率最大,此时正反应速率等于逆反应速率,故n点的逆反应速率最大,故答案为:b;m、n;n;
③由图可知,温度超过495℃时,乙二醇大量转化为CO2,使乙二醛的产率直线下降,故答案为:温度超过495℃时,乙二醇大量转化为CO2,使乙二醛的产率降低;
(2)HOOCCOOH与HOC-COOH对比,可知HOOCCOOH比HOC-COOH多一个O,HOOCCOOH
(3)①乙二醛溶液显中性,即起始溶液pH为7,因此图中曲线b表示溶液的pH值随时间变化的曲线,故答案为:b;
②将催化剂覆盖在纳米碳纤维上,可以增大接触面积,加快反应速率,故答案为:增大接触面积,加快反应速率;
③乙二醛(OHC-CHO)被氧气氧化生成乙醛酸(HOC-COOH),根据图象,最终乙二醛的浓度不为0,表示该反应为可逆反应,反应的化学方程式为:2OHC-CHO+O22HOC-COOH;由图可知,乙二醛起始浓度为5mol/L,8h后其浓度为2.5mol/L,则△c(OHC-CHO)=2.5mol/L,根据方程式,△c(HOC-COOH)=2.5mol/L,8h内乙醛酸的平均生成速率v(HOC-COOH)=![]() =0.3125mol/(Lh);根据图象,HOC-COOH的浓度为2.5mol/L时pH=1.5,则c(H+)=10-1.5mol/L,根据电离方程式HOC-COOHHOC-COO-+H+,c(HOC-COO-)=c(H+)=10-1.5mol/L,乙醛酸的电离常数Ka=
=0.3125mol/(Lh);根据图象,HOC-COOH的浓度为2.5mol/L时pH=1.5,则c(H+)=10-1.5mol/L,根据电离方程式HOC-COOHHOC-COO-+H+,c(HOC-COO-)=c(H+)=10-1.5mol/L,乙醛酸的电离常数Ka=![]() =
=![]() =4.0×10-4,故答案为:2OHC-CHO+O22HOC-COOH;0.3125mol/(Lh);4.0×10-4。
=4.0×10-4,故答案为:2OHC-CHO+O22HOC-COOH;0.3125mol/(Lh);4.0×10-4。