题目内容
【题目】完全燃烧一定质量的无水乙醇,放出的热量为Q,已知为了完全吸收生成的二氧化碳,消耗50mL 8mol/L的氢氧化钠溶液,则无水乙醇的燃烧放出的热量不可能是( )
A. 10Q B. 5Q~10Q C. 大于10Q或小于5Q D. 小于8Q
【答案】C
【解析】n(NaOH)=8mol/L![]() 0.05L=0.4mol;NaOH完全吸收CO2可能生成Na2CO3、NaHCO3、Na2CO3和NaHCO3的混合物;若只生成Na2CO3,反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,n(CO2)=
0.05L=0.4mol;NaOH完全吸收CO2可能生成Na2CO3、NaHCO3、Na2CO3和NaHCO3的混合物;若只生成Na2CO3,反应的化学方程式为CO2+2NaOH=Na2CO3+H2O,n(CO2)=![]() n(NaOH)=0.2mol;若只生成NaHCO3,反应的化学方程式为CO2+NaOH=NaHCO3,n(CO2)=n(NaOH)=0.4mol;乙醇完全燃烧生成的CO2物质的量:0.2mol
n(NaOH)=0.2mol;若只生成NaHCO3,反应的化学方程式为CO2+NaOH=NaHCO3,n(CO2)=n(NaOH)=0.4mol;乙醇完全燃烧生成的CO2物质的量:0.2mol![]() n(CO2)
n(CO2)![]() 0.4mol,则乙醇物质的量:0.1mol
0.4mol,则乙醇物质的量:0.1mol![]() n(CH3CH2OH)
n(CH3CH2OH)![]() 0.2mol;1mol无水乙醇燃烧放出的热量大于等于5Q(
0.2mol;1mol无水乙醇燃烧放出的热量大于等于5Q(![]() =5Q),小于等于10Q(
=5Q),小于等于10Q(![]() =10Q);不可能的是大于10Q或小于5Q,答案选C。
=10Q);不可能的是大于10Q或小于5Q,答案选C。

 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案【题目】下表是某兴趣小组通过实验获得的相同体积足量稀硫酸与铁反应的实验数据:
实验 序号 | 金属 质量/g | 金属 状态 | c(H2SO4) mol/L | 实验 温度/℃ | 金属消失 的时间/s |
1 | 0.10 | 丝 | 0.7 | 20 | 250 |
2 | 0.10 | 丝 | 1.0 | 20 | 200 |
3 | 0.10 | 粉末 | 1.0 | 20 | 125 |
4 | 0.10 | 粉末 | 1.0 | 30 | 50 |
分析上述数据,回答下列问题:
(1)①实验1、2可得出的结论是,硫酸浓度越_____,反应速率越慢;
②实验3、4可得出的结论是温度越_____,反应速率越快.
(2)①用铁粉和稀硫酸反应制取H2,实验过程中绘制出生成H2的体积(V)与时间(t)的关系如图所示. 试分析判断OE段、EF段、FG段、GH段反应速率(分别用v (OE)、v (EF)、v (FG)、v (GH)表示)最快时段是______.
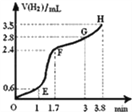
A.v (OE) B.v (EF)C.v (FG) D.v (GH)
②1min内反应较慢的原因是:_________;一段时间后反应明显加快的原因是_____.