题目内容
宋代著名法医学家宋慈的《洗冤集录》中有银针验毒的记载,“银针验毒”涉及的化学反应是 4Ag+2H2S+O2→2X+2H2O,下列说法正确的是
| A.X的化学式为AgS |
| B.银针验毒时,空气中氧气失去电子 |
| C.反应中Ag和H2S均是还原剂 |
| D.每生成1mo1X,反应转移2mo1电子 |
D
解析试题分析:A根据质量守恒定律可确定X的化学式是Ag2S。错误。B.银针验毒时,空气中氧气分子得到电子,化合价从反应前的0价变为反应后的H2O-2价。化合价降低。错误。C.在反应中Ag的化合价从单质Ag的0价变为反应后Ag2S中的+1价,失去电子,作还原剂; H2S中的H|S两元素的化合价都没有发生变化,故既不是氧化剂也不是还原剂。错误。D.在反应方程式中,产生 2molAg2S,转移电子4mol。所以生成1mo1Ag2S,反应转移2mo1电子。正确。
考点:考查《洗冤集录》中银针验毒的化学反应原理的知识。

 步步高达标卷系列答案
步步高达标卷系列答案在化学反应中,某元素由化合态变为单质,则该元素
| A.一定被氧化 | B.一定被还原 |
| C.既可能被氧化,也可能被还原 | D.以上都不是 |
代硫酸钠可用作脱氯剂,已知25.0 mL 0.1 mol·L-1的Na2S2O3溶液恰好把标准状况下112 mL Cl2完全转化为Cl-时,S2O32-转化成( )
| A.S2- | B.S | C.SO32- | D.SO42- |
将11.9 g Mg、Al、Fe组成的合金溶于足量NaOH溶液中,产生的气体在标准状况下体积为3.36 L。另取等质量合金溶于过量稀硝酸中,生成NO气体,向反应后的溶液中加入过量NaOH溶液,得到沉淀19.4 g,则上述反应中生成NO气体的体积为(标准状况下)
| A.6.72 L | B.11.2 L | C.22.4 L | D.4.48 L |
将反应 4(NH4)2SO4→ N2↑+6NH3↑+3SO2↑+SO3↑+7H2O 的产物气体通入BaCl2溶液,下列判断正确的是
| A.无沉淀生成 | B.肯定没有BaSO3生成 |
| C.得到的沉淀是纯净物 | D.得到的沉淀是BaSO4和BaSO3组成的混合物 |
PbO2是褐色固体,受热分解为Pb的+4和+2+4价的混合氧化物,+4价的Pb能氧化浓盐酸生成Cl2;现将1mol PbO2加热分解得到O2,向剩余固体中加入足量的浓盐酸得到Cl2,O2和Cl2的物质的量之比为3∶2,则剩余固体的组成及物质的量比是
| A.1∶1混合的Pb3O4、PbO |
| B.1∶2混合的PbO2、Pb3O4 |
| C.1∶4∶1混合的PbO2、Pb3O4、PbO |
| D.4∶1∶1混合的PbO2、Pb3O4、PbO |
已知酸性高锰酸钾溶液可以将FeSO4氧化,化学方程式为2KMnO4+10FeSO4+8H2SO4=K2SO4+2MnSO4+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液,混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示,
则下列有关说法中不正确的是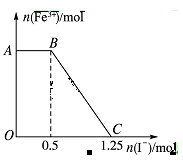
| A.图中AB段主要是高锰酸钾和碘化钾溶液反应 |
| B.图中BC段发生的反应为2Fe3++2I-=2Fe2++I2 |
| C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.25 mol |
| D.向C点以后的溶液中加入少量KSCN溶液,溶液变红色 |
下列化学变化中,必须加入氧化剂才能实现的是
| A.SO2→H2SO3 | B.Cl2→NaClO | C.Fe→FeCl2 | D.HNO3→O2 |