��Ŀ����
����Ŀ����һ���¶��£������� X ������ Y �� 0.16 mol ���� 10 L �����ܱ������У�������Ӧ��X(g)��Y(g) ![]() 2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
2Z(g) ��H��0��һ��ʱ���ﵽƽ�⡣��Ӧ�����вⶨ���������±���
t / min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
����˵����ȷ����( )
A.���¶��£��˷�Ӧ��ƽ�ⳣ�� K��1.44
B.4min ʱ����(��)����(��)
C.��Ӧǰ 2min ��ƽ������ ��(Z)��2.0��10��3mol/(L��min)
D.7min ʱ����Ӧ��δ�ﵽƽ��״̬
���𰸡�A
��������
A.�ɱ���֪��7minʱ��Ӧ�ﵽƽ�⣬ ���ݷ���ʽ��
X(g)��Y(g) ![]() 2Z(g)
2Z(g)
��ʼ��mol��0.16 0.16 0
ת����mol��0.06 0.06 0.12
ƽ�⣨mol��0.1 0.1 0.12
ƽ�ⳣ��K= 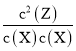 =
= ![]() =1.44����A��ȷ��
=1.44����A��ȷ��
B. 4min��Ӧ��û�дﵽƽ�⣬��(��) ����(��) ����B����
C. ��Ӧǰ 2min���ɵ�n��Y��=0.16mol-0.12mol=0.04mol�������ɵ�n��Z��=2 n��Y��=0.08mol��ƽ������ ��(Z)=  =4��10��3mol/(L��min)����C����
=4��10��3mol/(L��min)����C����
D. 7min��Y��Ũ�Ȳ��䣬˵��7minʱ��Ӧ�Ѿ��ﵽƽ�⣬��D����
��ȷ����A��

����Ŀ����0.48gþ�۷ֱ����10.0mL������Һ����Ӧ6Сʱ������ˮ���ռ���������������Һ�����H2���(�ѻ���ɱ�״��)�Ĺ�ϵ���±�������˵������ȷ����
ʵ�� | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
��Һ��� | H2O | 1.0mol/L NH4Cl | 0.1mol/L NH4Cl | 1.0mol/L NaCl | 1.0mol/L NaNO3 | 0.8mol/L NH4Cl+ 0.2mol/L NH3��H2O | 0.2mol/L NH4Cl+ 0.8mol/L NH3��H2O |
V/ml | 12 | 433 | 347 | 160 | 14 | 401 | 349 |
A.��ʵ��2��3�ɵã�![]() Ũ��Խ��þ��ˮ��Ӧ����Խ��
Ũ��Խ��þ��ˮ��Ӧ����Խ��
B.��ʵ��1��4��5�ɵã�Cl-��þ��ˮ�ķ�Ӧ�д�����
C.��ʵ��3��7�ɵã���Ӧ���̲�����Mg(OH)2������þ���棬������Ӧ
D.���������������Ǽ���������![]() ���ܼӿ�þ��ˮ�ķ�Ӧ
���ܼӿ�þ��ˮ�ķ�Ӧ
����Ŀ����֪![]() �£�������ĵ��볣�����£�
�£�������ĵ��볣�����£�
��ѧʽ |
| HCN |
|
���볣�� |
|
|
|
���и����ȷ����![]()
A.��NaCN��Һ��ͨ������![]() ��
��![]()
B.��̼������Һ�м��������![]()
C.��Ԫ����������ɵ�һ�������������Ϊ��һ����������������Ӷ���һ����������������
D.�����ʵ���Ũ�ȵ�![]() ��NaCN��Һ��NaCN��Һ�ļ��Ը�ǿ
��NaCN��Һ��NaCN��Һ�ļ��Ը�ǿ