题目内容
12.下列实验操作、现象和结论均正确的是( )| 选项 | 实验操作 | 现象 | 结论 |
| A | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
| B | 常温下将Fe片放入浓硝酸中 | 无明显变化 | Fe与浓硝酸不反应 |
| C | 将一小块Na放入医用酒精中 | 产生气泡 | Na只置换出醇羟基上的氢 |
| D | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Fe(OH)2易被氧化;
B.常温下将Fe片放入浓硝酸中,发生钝化;
C.Na与水、乙醇均反应生成氢气;
D.无色溶液中滴加氯水和CCl4,振荡、静置,下层溶液显紫色,则氯气与碘离子反应生成碘单质.
解答 解:A.Fe(OH)2易被氧化生成Fe(OH)3,则白色固体迅速变为灰绿色,最终变为红褐色,均合理,故A正确;
B.常温下将Fe片放入浓硝酸中,发生钝化,发生氧化还原反应,故B错误;
C.Na与水、乙醇均反应生成氢气,则结论不合理,故C错误;
D.无色溶液中滴加氯水和CCl4,振荡、静置,下层溶液显紫色,则氯气与碘离子反应生成碘单质,则原溶液中有I-,故D正确;
故选AD.
点评 本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、物质的性质、离子检验等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
2.下列有关化学表达式正确的是( )
| A. | 硫化氢的电子式: | B. | 甲醇的分子式:CH4O | ||
| C. | 氯原子的原子结构示意图: | D. | 丙烷的结构简式:C3H8 |
20.下列物质含有共价键的离子化合物的是( )
| A. | CaO | B. | CO2 | C. | NaOH | D. | CaCl2 |
7.化学与生活密切相关,下列说法不正确的是( )
| A. | 用热的纯碱溶液可洗涤餐具上的油污 | |
| B. | 煤经过气化和液化等物理变化可以转化为清洁燃料 | |
| C. | 用灼烧并闻气味的方法可区别棉麻织物和纯羊毛织物 | |
| D. | 新制Cu(OH)2悬浊液在医院中常用于尿糖的检测 |
17.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 1mol苯中含有3nA个碳碳双键 | |
| B. | 室温下,1LpH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA | |
| C. | 氢氧燃料电池正极消耗22.4L(标准状况)气体时,电路中通过的电子数目为2NA | |
| D. | 一定条件下2 mol SO2和1 mol O2充分反应后,混合气体的分子总数大于2NA |
4.X、Y、Z、W为周期表中前20号元素中的四种,原子序数依次增大,W、Y为金属元素,X原子的最外层电子数是次外层电子数的3倍,Y、Z位于同周期,Z单质是一种良好的半导体.W能与冷水剧烈反应,Y、Z原子的最外层电子数之和与X、W原子的最外层电子数之和相等.下列说法正确的是( )
| A. | 原子半径:W>Y>Z>X | |
| B. | 气态氢化物的稳定性:X<Z | |
| C. | 最高价氧化物对应水化物的碱性:Y<W | |
| D. | Y、Z的氧化物都有酸性和碱性 |
2.已知下表数据:
某学生做乙酸乙酯的制备实验
(1)写出该反应的化学反应式CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(2)按装置图安装好仪器后,在大试管中配制好体积比为3:2的乙醇和乙酸,加热至沸腾,很久也没有果香味液体生成,原因是漏加浓硫酸.
(3)根据上表数据分析,为什么乙醇需要过量一些,其原因是乙醇的沸点低,易挥发而损耗.
按正确操作重新实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物.现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图.在图中圆括号表示加入适当的试剂,编号表示适当的分离方法.
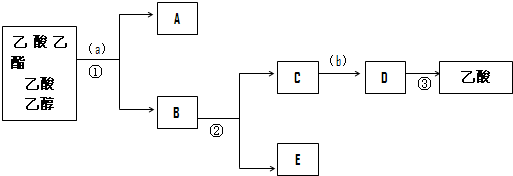
写出加入的试剂:试剂(a)是饱和碳酸钠;试剂(b)是稀硫酸溶液
写出有关的操作分离方法:①是分液,②是蒸馏,③是蒸馏.
(6)在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中混有的少量水.
| 物质 | 熔点/℃ | 沸点/℃ | 密度/(g/cm3) |
| 乙醇 | -144 | 78 | 0.789 |
| 乙酸 | 16.6 | 117.9 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0.90 |
| 浓硫酸 | -- | 338 | 1.84 |
(1)写出该反应的化学反应式CH3COOH+HOCH2CH3$?_{△}^{浓硫酸}$CH3COOCH2CH3+H2O.
(2)按装置图安装好仪器后,在大试管中配制好体积比为3:2的乙醇和乙酸,加热至沸腾,很久也没有果香味液体生成,原因是漏加浓硫酸.
(3)根据上表数据分析,为什么乙醇需要过量一些,其原因是乙醇的沸点低,易挥发而损耗.
按正确操作重新实验,该学生很快在小试管中收集到了乙酸乙酯、乙酸、乙醇的混合物.现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,如图是分离操作步骤流程图.在图中圆括号表示加入适当的试剂,编号表示适当的分离方法.

写出加入的试剂:试剂(a)是饱和碳酸钠;试剂(b)是稀硫酸溶液
写出有关的操作分离方法:①是分液,②是蒸馏,③是蒸馏.
(6)在得到的A中加入无水碳酸钠粉末,振荡,目的是除去乙酸乙酯中混有的少量水.
3.物质的量相同的下列各组有机物,充分燃烧耗氧量相同的一组是( )
| A. | C2H4 C2H6 | B. | C2H4 C3H6 | C. | C2H4 C2H6O | D. | C2H6O C2H4O2 |
 现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题:
现用如图装置来测定某原电池工作时在某段时间内通过导线的电子的物质的量.量筒的规格为1000mL,供选择的电极材料有纯铜片和纯锌片.请回答下列问题: