题目内容
下列实验现象及相关的离子方程式均正确的是( )
| A、碳酸钙粉末中加人醋酸溶液,固体逐渐减少,生成无色气体 CaCO3+2H+=Ca2++CO2↑+H2O | ||
| B、向BaCl2溶液中通人SO2气体,出现白色沉淀 Ba2++SO2+H2O=BaSO4↓+2H+ | ||
C、向H2O2溶液中滴加酸化的KMnO4溶液,KMnO4溶液褪色 2MnO
| ||
| D、将等物质的量浓度、等体积的Ba(OH)2溶液和NaHSO4溶液混合,生成白色沉淀 Ba2++SO42-+H++OH-=BaSO4↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.弱电解质写化学式;
B.二者不反应;
C.二者反应生成锰离子、氧气和水,转移电子不守恒;
D.二者反应生成硫酸钡、氢氧化钠和水.
B.二者不反应;
C.二者反应生成锰离子、氧气和水,转移电子不守恒;
D.二者反应生成硫酸钡、氢氧化钠和水.
解答:
解:A.弱电解质写化学式,离子方程式为CaCO3+2CH3COOH=Ca2++CO2↑+H2O+2CH3COO-,故A错误;
B.盐酸酸性大于亚硫酸,所以二者不反应,没有离子方程式,故B错误;
C.二者反应生成锰离子、氧气和水,转移到不守恒,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,故C错误;
D.二者反应生成硫酸钡、氢氧化钠和水,离子方程式为Ba2++SO42-+H++OH-=BaSO4↓+H2O,故D正确;
故选D.
B.盐酸酸性大于亚硫酸,所以二者不反应,没有离子方程式,故B错误;
C.二者反应生成锰离子、氧气和水,转移到不守恒,离子方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2↑,故C错误;
D.二者反应生成硫酸钡、氢氧化钠和水,离子方程式为Ba2++SO42-+H++OH-=BaSO4↓+H2O,故D正确;
故选D.
点评:本题考查了离子方程式正误判断,明确物质之间的反应、物质的性质及离子方程式书写规则是解本题关键,注意D中反应物的量,反应物的量不同其产物不同,为易错点.

练习册系列答案
相关题目
下列试剂中,不能贮存在玻璃瓶中的是( )
| A、浓硫酸 | B、氢氟酸 |
| C、浓氢氧化钠溶液 | D、硝酸银溶液 |
工业上用化学气相沉积法制备氮化硅,其反应如下:3SiCl4(g)+2N2(g)+6H2(g)
Si3N4(s)+12HCl(g)△H<0上述反应达到平衡后,下列说法正确的是( )
| ||
| A、其他条件不变时,增大Si3N4物质的量,平衡向左移动 |
| B、其他条件不变,增大压强,平衡常数K减小 |
| C、其他条件不变,增大H2物质的量,H2的转化率增大 |
| D、其他条件不变,移走部分HCl,逆反应速率先减小后增大 |
下列说法正确的是( )
| A、电子层结构相同的不同离子,其半径随核电荷数增大而减小 |
| B、C、O、S原子半径依次增大,氢化物稳定性逐渐增强 |
| C、ⅠA族元素与ⅦA元素形成的化合物都为离子化合物 |
| D、ⅦA族元素的阴离子还原性越强,其最高价氧化物对应水化物的酸性越强 |
下列表述中不正确的是( )
A、D
| ||
| B、12C和14C互为同位素,而C60与金刚石互为同素异形体 | ||
| C、一种原子的质量数为197,中子数为118,则它是主族元素 | ||
| D、一种元素的原子序数为m,另一种元素的原子序数为m+11,则这两种元素所在的族序数可能相邻 |
下列图象与对应的说法正确的是( )
A、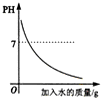 向NaOH溶液中加水稀释 |
B、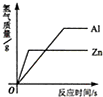 等质量的Al、Zn与足量的稀硫酸反应 |
C、 向稀硫酸中加入Ba(OH)2溶液 |
D、 恒温下,适量蒸发饱和NaCl溶液的水分 |