题目内容
【题目】(1)X、Y、Z三种物质存在如图所示转化。回答下列问题。
若X为黑色固体单质,A为O2,写出Z→Y的化学方程式_________________。
②若X为NaOH溶液,则写出Y→Z的化学方程式_______________________。
(2)已知常温下在溶液中可发生如下两反应:
Ce4++Fe2+=Fe3++Ce3+;Sn2++2Fe3+=2Fe2++Sn4+
由此可以确定Ce4+、Sn4+、Fe3+三种离子的氧化性由强到弱的顺序是 。
(3)Mn2+、Bi3+、BiO3-、MnO4-、H+、H2O组成的一个氧化还原反应体系中,发生BiO3-→Bi3+的反应过程。
①该反应中,被氧化的元素是_____________,氧化剂是_______________。
将以上物质分别填入下面对应的横线上,组成一个未配平的化学方程式。
________+ ______+ ________![]() ______+ ________+ H2O
______+ ________+ H2O
反应中若产生0.2mol的还原产物,则有_______mol电子转移。
【答案】(1)①CO2+C![]() 2CO;②CO2+Na2CO3+H2O=2NaHCO3;
2CO;②CO2+Na2CO3+H2O=2NaHCO3;
(2)Ce4+>Fe3+>Sn4+;
(3)①Mn,BiO3-;②BiO3-+Mn2++H+![]() Bi3++MnO4-+H2O;③0.4。
Bi3++MnO4-+H2O;③0.4。
【解析】
试题分析:(1)①X是黑色固体单质,因此X为C,Z为CO2,Y为CO,因此反应方程式为:CO2+C![]() 2CO;②X为NaOH,A为CO2,因此Y为Na2CO3,Z为NaHCO3,因此反应方程式N2CO3+CO2+H2O=2NaHCO3;(2)根据氧化剂的氧化性强于氧化产物的氧化性,Ce4+化合价降低,作氧化剂,Fe2+化合价升高,Fe3+作氧化产物,即Ce4+>Fe3+,Sn2+的化合价升高,作还原剂,Sn4+作氧化产物,Fe3+作氧化剂,Fe3+>Sn4+,因此有Ce4+>Fe3+>Sn4+;(3)①被氧化的元素,失去电子化合价升高,BiO3-→Bi3+,化合价降低,因此Mn的化合价升高,Mn被氧化,氧化剂是得到电子,化合价降低,即BiO3-作氧化剂;②根据①的分析,Mn2++BiO3-+H+→MnO4-+Bi3++H2O;③还原产物是Bi3+,转移电子物质的量为0.2×(5-3)mol=0.4mol。
2CO;②X为NaOH,A为CO2,因此Y为Na2CO3,Z为NaHCO3,因此反应方程式N2CO3+CO2+H2O=2NaHCO3;(2)根据氧化剂的氧化性强于氧化产物的氧化性,Ce4+化合价降低,作氧化剂,Fe2+化合价升高,Fe3+作氧化产物,即Ce4+>Fe3+,Sn2+的化合价升高,作还原剂,Sn4+作氧化产物,Fe3+作氧化剂,Fe3+>Sn4+,因此有Ce4+>Fe3+>Sn4+;(3)①被氧化的元素,失去电子化合价升高,BiO3-→Bi3+,化合价降低,因此Mn的化合价升高,Mn被氧化,氧化剂是得到电子,化合价降低,即BiO3-作氧化剂;②根据①的分析,Mn2++BiO3-+H+→MnO4-+Bi3++H2O;③还原产物是Bi3+,转移电子物质的量为0.2×(5-3)mol=0.4mol。

【题目】下列有关原子结构的说法,正确的是 ( )
A. 稀有气体元素原子的最外层电子数都是8 B. 非金属元素的最外层电子数都大于3
C. 金属元素的最外层电子数都小于4 D. 氢原子的电子云是球形对称的
【题目】苯甲酸广泛应用于制药和化工行业,某同学尝试用甲苯的氧化反应制备苯甲酸。反应原理:

己知甲苯的熔点为-95°C,沸点为110.6°C,易挥发,密度为0.866g/cm3;苯甲酸的熔点为122.4°C,在25°C和95°C下溶解度分别为0.3g和6.9g。
【制备产品】将30.0mL甲苯和25.0mLlmol/L高锰酸钾溶液在100°C下反应30min,装置如图所示。
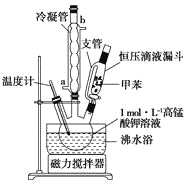
(1)图中冷凝管的进水口为________(填“a”或“b”)。支管的作用是___________。
(2)在本实验中,三领烧瓶最合适的容积___________(填字母)。
A.50mL | B.I00mL | C.200mL | D.250mL |
相对于用酒精灯直接加热,用沸水浴加热的优点是___________________。
【分离产品】该同学设计如下流程分离粗产品苯甲酸和回收甲苯
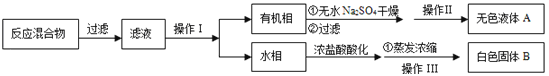
(3)操作Ⅰ的名称是 ;含有杂志的产物经操作Ⅱ进一步提纯得无色液体甲苯,则操作Ⅱ的名称是 。
(4)测定白色固体的熔点,发现其在115℃开始熔化,达到130℃时仍有少量不熔,该同学推测白色固体是苯甲酸与KCl的混合物,设计了如下方案进行提纯和检验,实验结果表明推测正确。请完成表中内容。
序号 | 实验方案 | 实验现象 | 结论 |
① | 将白色固体加入水中,加热溶解,______。 | 得到白色晶体和无色溶液 | |
② | 取少重滤液于试管中,________。 | 生成白色沉淀 | 滤液含Cl- |
③ | 干燥白色晶体,________。 | _____________________ | 白色晶体是苯甲酸 |
纯度测定:称取1.220g产品,配成100ml甲醇溶液,取25.00ml溶液,用0.1000mol/L KOH标准溶液滴定,重复滴定四次,每次消耗的体积如下表所示。
第一次 | 第二次 | 第三次 | 第四 | |
体积(mL) | 24.00 | 24.10 | 22.40 | 23.90 |
(5)滴定操作中,如果对装有KOH标准溶液的滴定管读数时,滴定前仰视,滴定后俯视则测定结果______________(填“偏大”、“偏小”或“不变”)。计算样品中苯甲酸纯度为______________。