题目内容
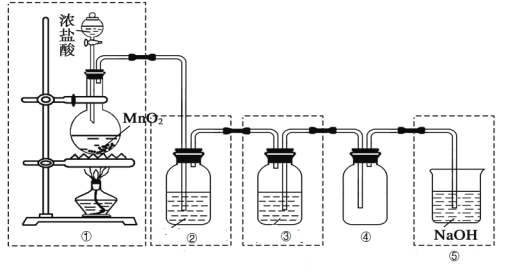
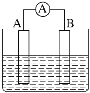
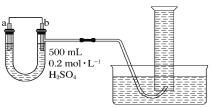
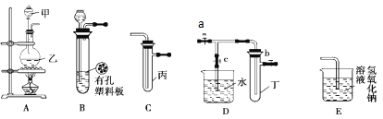
【题目】某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)A装置中甲仪器名称为______。
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
① A中乙为MnO2固体,甲中盛有浓盐酸,则烧瓶中发生反应的化学方程式为_____________。
② 若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行Ⅰ、Ⅱ两个实验,实验操作、现象结论如下:
Ⅰ. 将氯水滴入品红溶液中,现象________________。
Ⅱ. 氯水中加入 NaHCO3粉末,有无色气泡产生,某同学得出结论:氯气与水反应的产物具有较强的酸性。请你评价该同学的结论是否合理?若不合理,请说明理由。 ___________________
③E装置的作用__________________。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),关闭止水夹c,制得NO2,接着再进行有关实验。
① 欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹_____,再打开止水夹_____,使烧杯中的水进入试管丁的操作是_________________。
② NO2尾气可用NaOH溶液吸收生成两种钠盐,写出反应的化学方程式为____________。
【答案】分液漏斗 MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑ 溶液褪色 不合理,因为制取的氯气中含有HCl气体,HCl气体溶于水后能够与NaHCO3粉末反应产生气泡 吸收尾气,防止大气污染 a b c 双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流到试管丁 2NO2+2NaOH=NaNO2+NaNO3+H2O
MnCl2+2H2O+Cl2↑ 溶液褪色 不合理,因为制取的氯气中含有HCl气体,HCl气体溶于水后能够与NaHCO3粉末反应产生气泡 吸收尾气,防止大气污染 a b c 双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流到试管丁 2NO2+2NaOH=NaNO2+NaNO3+H2O
【解析】
(1)根据甲仪器特点分析。
(2)装置A、C、E构成了氯气的发生装置、收集装置、尾气处理装置。没有除杂装置,因此收集的Cl2中含有杂质HCl气体和水蒸气。
(3) 装置B、D、E构成了NO2的发生装置,收集装置和尾气处理装置,利用倒吸,使D烧杯中的水进入试管丁中。
(1)甲仪器示意图![]() ,名称为分液漏斗;
,名称为分液漏斗;
(2)①MnO2和浓盐酸在加热的条件下生成Cl2。化学方程式为MnO2+4HCl(浓)![]() MnCl2+2H2O+Cl2↑;
MnCl2+2H2O+Cl2↑;
②Ⅰ.氯气溶于水生成HCl和HClO,HClO具有漂白性,将氯水滴入品红溶液中,溶液会褪色;Ⅱ.盐酸具有挥发性,利用浓盐酸制备氯气的时候,氯气中的杂质包括HCl气体,而HCl气体溶于水后,可与NaHCO3反应有气泡产生。所以认为是氯气与水反应的产物具有较强的酸性,与NaHCO3反应是不合理的,答案为:不合理 ;因为制取的氯气中含有HCl气体,HCl气体溶于水后能够与NaHCO3粉末反应产生气泡;
③氯气有毒气体,会污染环境,E装置中盛装的是NaOH溶液,可以与氯气反应,因此E为尾气吸收装置,防止大气污染;
(3)①证明NO2和水反应,水要与NO2接触,将D烧杯中的水进入到试管丁中,应关闭止水夹a和b,使得不再有NO2进入和出去,打开止水夹c,利用热胀冷缩原理和NO2溶于水,引发倒吸,使水进入试管丁中。操作为:双手紧握(或微热)试管丁使试管中气体逸出,NO2与水接触后即可引发烧杯中的水倒流到试管丁;
②NO2用NaOH溶液吸收生成两种钠盐,NO2与NaOH发生歧化反应,N的化合价部分升高、部分降低,生成硝酸钠和亚硝酸钠,方程式为2NO2+2NaOH=NaNO2+NaNO3+H2O。

【题目】下表是周期表中的一部分,根据①--⑩在周期表中的位置,用元素符号或化学式回答下列问题:
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ④ | ⑦ | ⑧ | ⑩ | ||||
3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是______,还原性最强的单质是______,可用于制半导体材料的元素是______;
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是______;
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是______;
(4)铍![]() 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________。
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________。
【题目】以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工。
(1)将水蒸气通过红热的炭即可产生水煤气。反应为C(s)+H2O(g)CO(g)+H2(g) ΔH=+131.3 kJ·mol-1。
①该反应在常温下_______(填“能”或“不能”)自发进行。
②一定温度下,在一个容积可变的密闭容器中,发生上述反应,下列能判断该反应达到化学平衡状态的是____(填字母,下同)。
a.容器中的压强不变
b.1 mol H—H键断裂的同时,断裂2 mol H—O键
c.c(CO)=c(H2)
d.密闭容器的容积不再改变
(2)将不同量的CO(g)和H2O(g)分别通入体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g)CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
H2O | CO | H2 | CO | |||
1 | 650 | 2 | 4 | 1.6 | 2.4 | 6 |
2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验1中从反应开始至平衡以CO2表示的平均反应速率为v(CO2)=________(取小数点后两位,下同)。
②该反应的正反应为________(
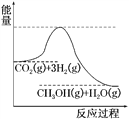
(3)目前工业上有一种方法是用CO2来生产甲醇。一定条件下发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ·mol-1)的变化。在体积为1 L的恒容密闭容器中,充入1 mol CO2和3 mol H2,达到平衡后下列措施中能使c(CH3OH)增大的是________。
a.升高温度
b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来
d.再充入1 mol CO2和3 mol H2
【题目】无水氯化铝在生产、生活中应用广泛。
(1)氯化铝水溶液呈_____性,原因是(用离子方程式表示)________;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______。
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
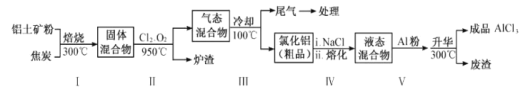
已知:
物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是___________(只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是_____。
③ 已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1kJ ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2kJ ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为______________。
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为_______、 _______ 、 _________。
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是___________________。