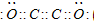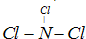题目内容
现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构.已知:
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
P
Q
M+P
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)C元素在周期表的位置
 .
.
(2)A元素的原子结构示意图是
 .化合物X所含化学键类型有
.化合物X所含化学键类型有
(3)G气体的检验方法为
(4)E的非金属性比F
①常温下,F的单质是一种有色气体,常用于杀菌、消毒;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同主族元素,氢化物(H2E)常温下为气态.
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y.
请回答下列问题:
(1)C元素在周期表的位置
N元素处于第二周期、ⅤA族
N元素处于第二周期、ⅤA族
;B2E的电子式为

(2)A元素的原子结构示意图是


离子键和共价键
离子键和共价键
.(3)G气体的检验方法为
将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可)
将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可)
.(4)E的非金属性比F
弱
弱
(填“强”或“弱”),并用化学事实加以说明(用化学方程式表示)H2S+Cl2=S+2HCl(其他合理答案也可)
H2S+Cl2=S+2HCl(其他合理答案也可)
.分析:现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构,①常温下,F的单质是一种有色气体,常用于杀菌、消毒,则F是Cl元素;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸,则A是Al元素;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
P
Q
M+P,则C是N元素;
④E和D是同主族元素,氢化物(H2E)常温下为气态,则E是S元素,D是O元素;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y,则B是Na元素.
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸,则A是Al元素;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同主族元素,氢化物(H2E)常温下为气态,则E是S元素,D是O元素;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y,则B是Na元素.
解答:解:现有A、B、C、D、E、F六种短周期元素,在化学反应中均能形成简单的阴离子或阳离子,且A、B、C、D离子具有相同的电子层结构,①常温下,F的单质是一种有色气体,常用于杀菌、消毒,则F是Cl元素;
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸,则A是Al元素;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
P
Q
M+P,则C是N元素;
④E和D是同主族元素,氢化物(H2E)常温下为气态,则E是S元素,D是O元素;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y,则B是Na元素,
(1)C是N元素,N元素处于第二周期、ⅤA族,硫化钠的电子式为: ,
,
故答案为:N元素处于第二周期、ⅤA族; ;
;
(2)A是Al元素,其原子结构示意图为: ,X是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键,
,X是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键,
故答案为: ;离子键和共价键;
;离子键和共价键;
(3)G是氨气,氨气能使湿润的红色石蕊试纸变蓝色,所以氨气的检验方法是:将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可),
故答案为:将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可);
(4)同一周期中,元素的非金属性随着原子序数的增大而增强,硫和氯元素处于同一周期,且氯元素的原子序数大于硫元素,所以硫的非金属性比氯元素弱,氯气和硫化氢能发生置换反应,反应方程式为:H2S+Cl2=S+2HCl(其他合理答案也可),
故答案为:弱;H2S+Cl2=S+2HCl(其他合理答案也可).
②A的氧化物既能溶于NaOH溶液,又能溶于盐酸,则A是Al元素;
③C的氢化物分子G是具有10电子的微粒,且可以发生下列转化:G
| D的单质 |
| D的单质 |
| H2O |
④E和D是同主族元素,氢化物(H2E)常温下为气态,则E是S元素,D是O元素;
⑤B和D可形成微粒个数比为1:1和2:1的离子化合物X和Y,则B是Na元素,
(1)C是N元素,N元素处于第二周期、ⅤA族,硫化钠的电子式为:
 ,
,故答案为:N元素处于第二周期、ⅤA族;
 ;
;(2)A是Al元素,其原子结构示意图为:
 ,X是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键,
,X是过氧化钠,过氧化钠中钠离子和过氧根离子之间存在离子键,氧原子和氧原子之间存在共价键,故答案为:
 ;离子键和共价键;
;离子键和共价键;(3)G是氨气,氨气能使湿润的红色石蕊试纸变蓝色,所以氨气的检验方法是:将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可),
故答案为:将湿润的红色石蕊试纸靠近气体,若试纸变蓝,则该气体为NH3(其他合理答案也可);
(4)同一周期中,元素的非金属性随着原子序数的增大而增强,硫和氯元素处于同一周期,且氯元素的原子序数大于硫元素,所以硫的非金属性比氯元素弱,氯气和硫化氢能发生置换反应,反应方程式为:H2S+Cl2=S+2HCl(其他合理答案也可),
故答案为:弱;H2S+Cl2=S+2HCl(其他合理答案也可).
点评:本题考查了元素化合物的性质,正确推断元素是解本题关键,注意氨气、常见离子的检验方法,为常考查点.

练习册系列答案
相关题目
 现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.
现有A、B、C、D、E、F六种短周期元素,它们的原子序数依次增大,D与E的氢化物分子构型都是V型.A、B的最外层电子数之和与C的最外层电子数相等,A能分别与B、C、D形成电子总数相等的分子,且A与D可形成的化合物,常温下均为液态.