题目内容
6.下列实验操作、现象和结论均正确的是( )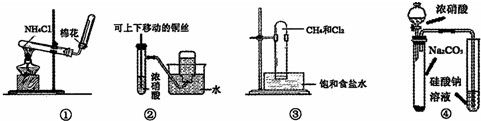
| 选项 | 操作 | 现象 | 结论 |
| A | ①将湿润的红色石蕊试纸靠近试管口 | 试纸不变色 | NH4Cl受热不分解 |
| B | ②将铜丝向下移动使其与浓硝酸接触 | 产生红棕色气体,用排水法收集气体 | 可以用该装置制备NO2 |
| C | ③光照 | 试管颜色变浅,出现油状滴液,少量白雾 | 甲烷与氯水发生取代反应 |
| D | 打开分液漏斗 | 右侧试管中出现白色沉淀 | 酸性:HNO3>H2CO3>H2SiO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯化铵分解后,在试管口又化合生成氯化铵;
B.Cu与浓硝酸反应生成二氧化氮,二氧化氮与水反应;
C.光照下甲烷与氯气发生取代反应,生成的HCl易结合水蒸气形成酸雾;
D.浓硝酸易挥发,硝酸可与硅酸钠反应.
解答 解:A.氯化铵分解后,在试管口又化合生成氯化铵,不能只利用氯化铵制备氨气,故A错误;
B.Cu与浓硝酸反应生成二氧化氮,二氧化氮与水反应,则产生红棕色气体,但不能用排水法收集二氧化氮气体,故B错误;
C.光照下甲烷与氯气发生取代反应,生成的HCl易结合水蒸气形成酸雾,则操作、现象和结论均合理,故C正确;
D.浓硝酸易挥发,硝酸可与硅酸钠反应,图中装置不能比较H2CO3、H2SiO3的酸性,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,涉及物质的制备、气体的收集、酸性比较等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验装置的作用及实验评价性分析,题目难度不大.

练习册系列答案
 中考利剑中考试卷汇编系列答案
中考利剑中考试卷汇编系列答案
相关题目
1.已知:NO2(g)+SO2(g)$\frac{\underline{\;一定条件\;}}{\;}$SO3(g)+NO(g),现将体积之比为1:2的NO2和SO2的混合气体置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是( )
| A. | 体系压强保持不变 | B. | 混合气体颜色保持不变 | ||
| C. | SO3与NO的体积比保持不变 | D. | 每消耗1molSO2,同时生成1molNO |
11.下列图示与对应的叙述相符的是 ( )
| A. |  表示某吸热反应分别在有、无催化剂的情兄下反应过程中的能量变化 | |
| B. |  表示常温下,0.1 OOOmoi/LNaOH 溶液液滴定 20.00mL、0.0100/LHCl 溶液 所得到的滴定曲线 | |
| C. | 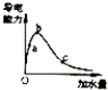 表示一定质量的冰醋酸加水稀释过程中,醋酸溶液电离程度:c>a>b | |
| D. |  表示反应4CO+2NO2(g)?N2(g)+4CO2(g),在其他条件不变的情况下改变起始物CO的物质的量,平衡时N2的体识分数变化情况,由图可知NO2的转化率 c>b>a |
18.煤气化过程中生成的CO和H2一定条件下制甲醇的反应如下:CO(g)+2H2(g)?CH3OH(g)△H<0.其他条件不变,改变某一条件后,用示意图表示的反应变化正确的是( )
| A | B | C | D | |
| 改变的条件 | 压强 | 温度 | 平衡体系增加H2 | 催化剂 |
| 变化的示意图 | 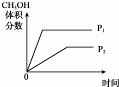 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
15.25℃时,下列分子或离子在指定的分散系中能大量共存的一组是( )
| A. | 空气 SO2、NO、NO2、CO | |
| B. | 碱性溶液 Na+、K+、NO3-、CO32- | |
| C. | 酸性溶液 Na+、ClO-、SO42-、SiO32- | |
| D. | KNO3溶液 Fe2+、H+、Cl-、Cu2+ |