题目内容
10.某烃分子中碳的质量分数为83.33%,它对氢气的相对密度是36,其一氯代物只有一种,通过计算推断出该烃的分子式和结构简式.分析 相对密度与相对分子质量成正比,据此计算出该烃的相对分子质量,再结合该烃分子中的含碳量计算出其含有的C原子数,然后结合其分子量计算出含有H原子数,从而可确定其分子式;其一氯代物只有1种,说明其分子中结构对称,中含有1种H原子,结合其分子式写出其结构简式.
解答 解:该烃对氢气的相对密度是36,则该烃的相对分子质量为:2×36=72,
该烃分子中碳的质量分数为83.33%,则其分子中含有C原子数为:N(C)=72×83.331272×83.3312≈5,
则该烃分子中含有H原子数为:N(H)=72−12×5172−12×51=12,
所以烃的分子式为:C5H12,为戊烷,
又一氯代物只有一种,则该戊烷分子中所有C原子都等效,该有机物为新戊烷,其结构简式为 ,
,
答:该烃的分子式为C5H12,结构简式为 .
.
点评 本题考查了有机物分子式、结构简式的确定,题目难度中等,明确相对密度与相对分子质量的关系为解答关键,注意掌握质量守恒定律在确定有机物分子式中的应用,还要明确同分异构体的概念及书写原则.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
20.下列叙述中正确的是( )
| A. | 化学反应中物质变化的实质是旧化学键的断裂和新化学键的形成 | |
| B. | 离子化合物中一定有金属元素和非金属元素 | |
| C. | 全部由非金属元素形成的化合物一定是共价化合物 | |
| D. | 共价化合物中各原子都一定满足最外层8电子稳定结构 |
1.在指定环境中,下列各组离子一定能够大量共存的是( )
| A. | 在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl- | |
| B. | 使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ | |
| C. | 加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- | |
| D. | 在c(H+)c(OH−)c(H+)c(OH−)=1×1013的溶液中:NH4+、Ca2+、C1-、K+ |
18.下列变化中,属于化学变化的是( )
| A. | 石油分馏 | B. | 碘片升华 | C. | 食盐熔化 | D. | 煤的干馏 |
5.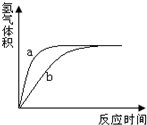 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
 将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )
将质量和形状相同的两小块金属钠分别投入足量水和足量无水乙醇中,产生氢气的体积和反应时间的关系如图所示,则( )| A. | a表示水,b表示无水乙醇 | B. | a表示无水乙醇,b表示水 | ||
| C. | 都可用a曲线表示 | D. | 都可用b曲线表示 |
15.下列俗名和化学式配对错误的是 ( )
| A. | 明矾→KAlSO4•12H2O | B. | 重晶石→BaSO4 | ||
| C. | 熟石膏→2CaSO4•H2O | D. | 硫磺→S |
2.下列试剂保存方法错误的是( )
| A. | 少量白磷保存在水里 | |
| B. | 钠保存在煤油里 | |
| C. | 液溴保存在棕色玻璃瓶里且覆盖一层水 | |
| D. | 装氢氟酸的玻璃瓶用橡皮塞 |
19.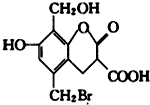 某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )
某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )
 某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )
某有机物的结构简式如图,取足量的Na、NaOH 溶液和NaHCO3溶液分别和等物质的量的该有机物在一定的条件下反应(必要时可以加热),完全反应后消耗Na、NaOH和 NaHCO3三种物质的物质的量之比为( )| A. | 3:4:2 | B. | 3:5:2 | C. | 3:5:1 | D. | 3:4:1 |
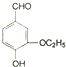 )是食品添加剂的增香原料,其香味比香草醛更加浓郁.
)是食品添加剂的增香原料,其香味比香草醛更加浓郁.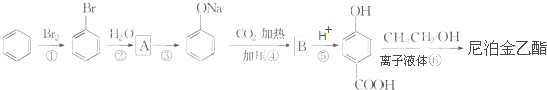
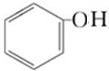 ,B
,B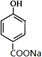 ;
;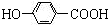 +CH3CH2OH
+CH3CH2OH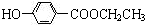 +H2O.
+H2O.