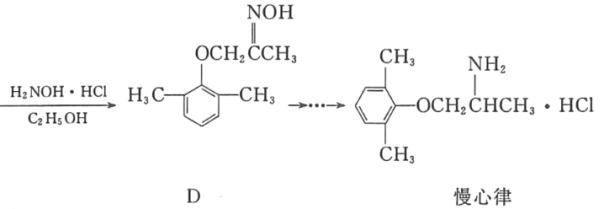
题目内容
【题目】某工厂的工业废水中含有大量的FeSO4和较多的Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收FeSO4和金属铜。请根据以下流程图,回答下列问题。
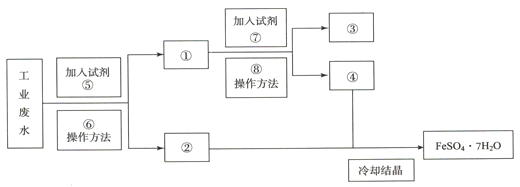
(1)写出下列标号所代表的物质的名称(注意用量)或操作方法③_____,⑥_____。
(2)鉴别溶液④中的金属阳离子时,应滴加的试剂依次是______,现象依次是_______,并写出对应反应的离子方程式:_______,______。
(3)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,此过程涉及的氧化还原反应的化学方程式是__________。
【答案】铜 过滤 氯水和KSCN溶液 溶液先由浅绿色变为黄色,加入KSCN溶液后变为红色 2Fe2++Cl2=2Fe3++2Cl- Fe3++3SCN-=Fe(SCN)3 4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
工业废水中含大量FeSO4、Cu2+,从该废水中回收硫酸亚铁和金属铜,结合流程可知,向废水中加入过量的Fe,与Cu2+发生置换反应产生Cu和Fe2+,经过滤后分离得到的滤渣中含有Fe、Cu,滤液中含有FeSO4;向滤渣中加入足量稀H2SO4,Fe与硫酸反应产生FeSO4和H2,Cu不能发生反应,仍然以固体形式存在,经过滤后,滤液与第一次过滤得到的滤液合并,然后经蒸发、浓缩、结晶、过滤,可得到FeSO4·7H2O,以此来解答。
(1)根据上述分析可知:③是Cu单质;⑥是过滤;
(2)④是FeSO4溶液,检验Fe2+的方法是:取少量④溶液,向其中滴加几滴新制氯水,溶液先由浅绿色变为黄色,然后再滴加2滴KSCN溶液,溶液变为血红色,就证明溶液中含有Fe2+,反应对应的离子方程式为:2Fe2++Cl2=2Fe3++2Cl-、Fe3++3SCN-=Fe(SCN)3;
(3)若取2mL溶液④加入试管中,然后滴加氢氧化钠溶液,发生反应:Fe2++2OH-=Fe(OH)2↓,Fe(OH)2不稳定,容易被溶解在溶液中的氧气氧化产生Fe(OH)3,此过程涉及的氧化还原反应的化学方程式是4Fe(OH)2+O2+2H2O=4Fe(OH)3。所以看到的实验现象是:产生白色沉淀,沉淀迅速变为灰绿色,最后变为红褐色。

 全能测控期末小状元系列答案
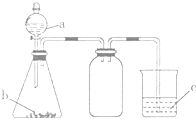
全能测控期末小状元系列答案【题目】利用如图所示的仪器和药品(必要时可加热),能够达到实验目的是( )
试剂a | 试剂b | 试剂c | 实验目的 |
| |
① | 盐溶液X | NaOH | 酚酞 | 证明X中含有NH4+ | |
② | 浓盐酸 | CaCO3 | Na2SiO3溶液 | 证明酸性: HCl>H2CO3>H2SiO3 | |
③ | 浓盐酸 | MnO2 | 淀粉KI溶液 | 证明氧化性:MnO2>Cl2>I2 | |
④ | 浓硫酸 | C | 澄清石灰水 | 证明产物中含有CO2 |
A.①②③B.①③C.②③D.①②③④