题目内容
7.纯水中c(H+)=5.0×10-7mol/L,则此时纯水中的c(OH-)=5.0×10-7mol/L;若温度不变,滴入稀硫酸使c(H+)=5.0×10-3mol/L,则c(OH-)=5.0×10-11mol/L.分析 根据纯水中c(OH-)=c(H+),溶液显示中性进行分析;
根据该温度下纯水中氢离子浓度和氢氧根离子浓度,计算出水的离子积,根据水的离子积计算出溶液中氢氧根离子的浓度,酸性溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度.
解答 解:纯水显示中性,c(OH-)=c(H+)=5.0×10-7mol/L;
此温度下,水的离子积为:Kw=5.0×10-7×5.0×10-7=2.5×10-13,
溶液中氢离子浓度c(H+)=5.0×10-3mol/L,c(OH-)=$\frac{2.5×1{0}^{-13}}{5.0×1{0}^{-3}}$mol/L=5.0×10-11 mol/L,
酸性溶液中水电离出的氢离子浓度等于溶液中氢氧根离子浓度,由水电离出的c(H+)=5.0×10-11 mol/L,
故答案为:5.0×10-7mol/L;5.0×10-11mol/L.
点评 本题考查了水的离子积常数的有关计算,注意水的离子积常数只与温度有关,与溶液的酸碱性无关,为易错点.

练习册系列答案
相关题目
2.NA为阿伏加德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4L H2O含有的分子数为NA | |
| B. | 一定条件下,56克铁粉与足量的HCl溶液完全反应,转移电子数为3NA | |
| C. | 标准状况下,22.4L氦气中所含原子数为NA | |
| D. | 1 mol•L-1 NaCl溶液中所含有的Na+离子数目为NA |
19.标准状况下,与16gO2所占体积大致相等的是( )
| A. | 0.5molH2O | B. | 5.6L甲烷 | C. | 3.01×1023个N2 | D. | 44gCO2 |
16.在无色透明溶液中,能大量共存的离子组是( )
| A. | K+ Cu2+ Na+ SO42- | B. | Mg2+ Cl- OH- SO42- | ||
| C. | K+ H+ NO3- CO32- | D. | Na+ Cl- NO3-CO32- |
 .
.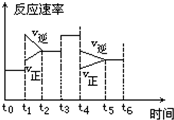 在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图:
在一密闭体系中发生下列反应:N2+3H2?2NH3 △H<0,如图是某一时间段中反应速率与反应进程的曲线关系图: