题目内容
【题目】对某溶液中部分离子的定性检测流程如下。相关分析正确的是
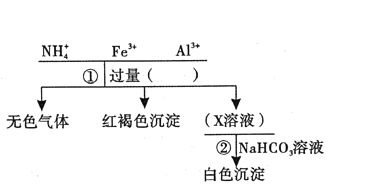
A. 步骤①所加试剂可以是浓NaOH溶液
B. 可以用湿润的蓝色石蕊试纸检验生成的无色气体
C. 红褐色沉淀与HI反应的离子方程式为:Fe(OH)3+3H+=Fe3++3H2O
D. 步骤②的反应为:Al3++3HCO3-=Al(OH)3↓+CO2↑
【答案】A
【解析】
A. 无色气体为氨气,红褐色沉淀为氢氧化铁,X溶液为偏铝酸钠溶液,所以步骤①所加试剂可以是浓NaOH溶液,故A正确;
B. 应该用湿润的红色石蕊试纸检验氨气,故B错误;
C. ![]() 可以氧化I-生成I2,故C错误;
可以氧化I-生成I2,故C错误;
D. 步骤②的反应为:AlO2- + HCO3- + H2O = CO32- + Al(OH)3↓,故D错误;
故选A。

 一线名师提优试卷系列答案
一线名师提优试卷系列答案【题目】工业上利用合成气(CO、CO2和H2)来生产甲醇,有关反应的化学方程式及其在不同温度下的化学平衡常数如下表所示。
化学反应 | 平衡 常数 | 温度/℃ | ||
500 | 700 | 800 | ||
①2H2(g)+CO(g)CH3OH(g)△H1 | K1 | 2.5 | 0.34 | 0.15 |
②H2(g)+CO2(g)H2O(g)+CO(g)△H2 | K2 | 1.0 | 1.70 | 2.52 |
③3H2(g)+CO2(g)CH3OH(g)+H2O(g)△H3 | K3 | |||
(1)若合成气为H2和CO2,发生反应III。
①由H2(g)和CO2(g)合成CH3OH(g)的△H3=___________。(用△H1、△H2表示)
②下列措施能使反应III的平衡体系中n(CH3OH)/n(H2)增大的是___________(填字母代号)
A.将水蒸气从体系中分离出去 B.恒压时充入氦气
C.升高温度 D.恒容时再充入一定量CO2
③500℃测得反应Ⅲ在10分钟时,H2(g)、CO2(g)、CH3OH(g)、H2O(g)的浓度分別为2mol·L-1、1.0 mol·L-1、0.6 mol·L-1、0.6 mol·L-1,则此时v(正)___________V(逆)(填“>”“=”或“<”)。从开始到该时刻,用H2表示反应的平均速率为v(H2)=___________。
(2)用合成气H2、CO和CO2生产甲醇。当n(H2)/n(CO+CO2)=a时,体系中CO平衡转化率[α(CO)]与温度和压强关系的一些散点如图所示。520K压强为P时,α(CO)处于C点,

①若保持温度不变,增大压强,则可能是图中的___________点(填字母,下同)。
②若保持压强不变,升高温度,则可能是图中的___________点。
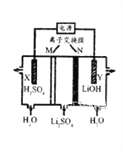
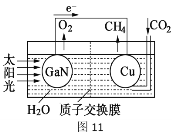
(3)利用甲醇燃料电池进行电解的装置如图1,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后断开K,此时AB两极上生成等物质的量的气体。
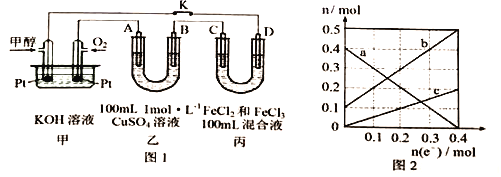
①乙中B电极为___________(填“阴极”或“阳极”),该电极上生成的气体在标准状况下的体积为___________;
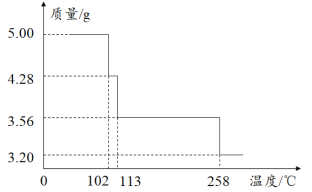
②丙装置溶液中金属阳离子的物质的量(n)与转移电子的物质的量[n(e-)]变化关系如图2,则图中c线表示的是___________(填离子符号)的变化。
【题目】实验能力和创新意识是化学学科核心素养的重要内容之一。某研究性学习小组在验证反应“ Fe![]() ”的实验中检测到
”的实验中检测到![]() 发现和探究过程如下:向硝酸酸化的
发现和探究过程如下:向硝酸酸化的![]() 硝酸银溶液(
硝酸银溶液(![]() )中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
)中加入过量铁粉,搅拌后静置,烧杯底部有黑色固体,溶液呈黄色。
(1)检验产物:
①检验上层清液中所含离子的方法:取上层清液,滴加_________,产生蓝色沉淀,说明溶液中含有Fe2+。
②经检验黑色固体为Ag,检验方法:取出少量黑色固体,洗涤后,加入适量稀硝酸使固体溶解,再滴加__________(填试剂),产生_________(填现象)。
(2)针对“溶液呈黄色”,甲认为溶液中有![]() 乙认为铁粉过量时不可能有
乙认为铁粉过量时不可能有![]() ,乙依据的原理是______。(用离子方程式表示)o
,乙依据的原理是______。(用离子方程式表示)o
针对这两种观点继续实验:取上层清液,滴加KSCN溶液,溶液变红,证实了甲的猜测。同时发现有白色沉淀产生,且溶液颜色深浅、沉淀量多少与取样时间有关,对比实验记录如下:
序号 | 取样时间/min | 现象 |
I | 3 | 产生大量白色沉淀;溶液呈红色 |
II | 30 | 产生白色沉淀,较3 min时量少;溶液红色较3 min时加深 |
III | 120 | 产生白色沉淀,较30min时量少;溶液红色较30min时变浅 |
(资料: ![]() -生成白色沉淀AgSCN)
-生成白色沉淀AgSCN)
(3)实验中溶液变为红色的离子方程式为_______________,产生白色沉淀说明存在___________(填离子符号)。
(4)对![]() 产生的原因做如下假设:
产生的原因做如下假设:
假设a:可能是铁粉表面有氧化层,能产生![]()
假设b:空气中存在![]() 发生反应
发生反应![]() 产生
产生![]()
假设c:酸性溶液中的NO3-将Fe2+氧化为Fe3+
假设d
下述实验可证实假设a、b,c不是产生Fe3+的主要原因,并可证实假设d成立。
①实验:向硝酸酸化的__________溶液( ![]() )中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液。3min 时溶液呈浅红色,30min后溶液几乎无色。
)中加入过量铁粉,搅拌后静置,不同时间取上层清液滴加KSCN溶液。3min 时溶液呈浅红色,30min后溶液几乎无色。
②实验II的现象说明发生了反应__________(用离子方程式表示)。
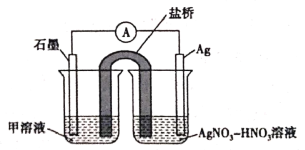
(5)实验Ⅱ中发生的反应可以用下列装置来验证。其中甲溶液是___________,分别取电池工作前与工作一段时间后左侧烧杯中溶液,同时滴加KSCN溶液,_______ (“前者”或“后者”)红色更深。