��Ŀ����
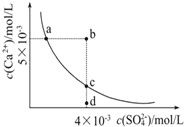
����Ŀ��������(SrSO4)�������̻���մɹ�ҵ���������ǿ�������ʯ����Ҫ�ɷ֣�����Na2SO4��Һ����������Һ�������á���ͼ�������ȵ��ܽ����ߣ�����˵����ȷ����

A. ͼ����a��c������ܶȻ���Ksp(a)<Ksp(c)
B. 363Kʱ���ܶȻ�Ksp(SrSO4)=1.0��10-3.20
C. SrSO4���ܽ�����¶����߶�����
D. 313Kʱ��b��Ϊ������Һ��d��Ϊ��������Һ
���𰸡�B
��������A���ܶȻ�ֻ���¶ȵ�Ӱ�죬�¶Ȳ��䣬���ܶȻ����䣬��Ksp(a)=Ksp(c)���ʴ���B��Ksp=c(Sr2��)��c(SO42��)��c(Sr2��)=10��1.6mol��L��1��c(SO42��)=10��1.6mol��L��1����Ksp=10��1.6��10��1.6=10��3.2������ȷ��C�����ݱ������ݣ��ó�Ksp�Ĵ�С˳����313K>283K>363K���ʴ���D��b���c(Sr2��)��c(SO42��)<Ksp��˵��b��û�дﵽ���ͣ�ͬ��d��Ϊ��������Һ���ʴ���

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��Ϊ��Ч�������������ػ�����ȡ��ʩ���ƴ������������У����ƿ����е����������������ĺ�����Ϊ��Ҫ��
(1)úȼ�ղ����������к��е���������,��CH4����ԭNO2�����������������Ⱦ����֪��
��CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ��H= -867.0kJ/mol��
��N2(g)+2O2(g)=2NO2(g) ��H=+67.8kJ/mol��
��N2(g)+O2(g)=2NO(g) ��H=+89.0kJ/mol
��CH4����ԭNO���Ȼ�ѧ����ʽΪ_______��
(2)��0.20mol NO��0.10mol CO����һ���¶Ⱥ㶨���ݻ���Ϊ2L���ܱ������з�����Ӧ2NO(g)+2CO(g)=N2(g)+2CO2(g)����ʵ�ֵ��������ת������Ӧ�����в������ʵ����ʵ����仯��ͼ��ʾ��
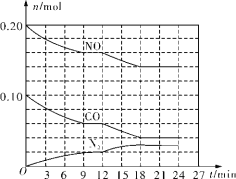
��N2��0��9min�ڵ�ƽ����Ӧ����v(N2)��________mol/(L��min)(������λ��Ч����)��
����12minʱ�ı�ķ�Ӧ��������Ϊ________(����ĸ����)��
a������ˮ����ϡ�ͷ�Ӧ�� b������NO c���Ӵ��� d������ѹǿ
(3)�����£������е�SO2����ijŨ�ȵ�NaOH��Һ���յõ�pH=7����Һ���Լ���������Һ��![]() ��_____(��֪:������H2SO3�ĵ���ƽ�ⳣ��Ka1=1.0��10-2��Ka2=6.0��10-8)��
��_____(��֪:������H2SO3�ĵ���ƽ�ⳣ��Ka1=1.0��10-2��Ka2=6.0��10-8)��
(4)�����е�SO2Ҳ����Na2SO3��Һ���գ����չ����У�pH��n(SO32-):n(HSO3-)�仯��ϵ���±���
n(SO32-):n(HSO3-) | 99��1 | 1��1 | 1��99 |
pH | 8.2 | 7.2 | 6.2 |
������Һ������ʱ����Һ������Ũ�ȹ�ϵ��ȷ����(ѡ����ĸ): ___________
a��c(Na��)=2c(SO32-)��c(HSO3-)
b��c(Na��)>c(HSO3-)>c(SO32-)>c(H��)=c(OH-)
c��c(Na��)+c(H+) =c(SO32-)+c(HSO3-)+c(OH-)