题目内容
某元素原子价电子构型3d54S2,其应在周期表( )
| A.第四周期ⅡA族 | B.第四周期ⅡB族 |
| C.第四周期ⅦA族 | D.第四周期ⅦB族 |
D
解析试题分析:根据元素原子价电子构型3d54S2可知,该元素应在周期表的第四周期ⅦB族,答案选D。
考点:考查价电子的应用以及元素周期表的结构
点评:该题是常识性知识的考查,难度不大。明确价电子的含义、周期数与族序数的判断依据是答题的关键,有利于调动学生的学习兴趣,激发学生的学习积极性。

练习册系列答案
相关题目
下列不能说明氯的非金属性比硫强的事实是 ( )
①HCl比H2S稳定 ②HCl和H2S的水溶液前者的的酸性强
③HClO4酸性比H2SO4强 ④Cl2能与H2S反应生成S
⑤Cl原子能得1个电子变成稳定离子而S原子能得两个电子
⑥Cl2与Fe反应生成FeCl3,S与Fe反应生成FeS
| A.①②④ | B.① ②⑥ | C.②⑤ | D.①③⑤ |
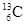 -NMR(核磁共振)可以用于含碳化合物的结构分析。
-NMR(核磁共振)可以用于含碳化合物的结构分析。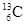 表示的碳原子
表示的碳原子
| A.核外有13个电子,其中4个能参与成键 |
| B.核内有6个质子,核外有7个电子 |
| C.质量数为13,原子序数为6,核内有7个质子 |
| D.质量数为13,原子序数为6,核内有7个中子 |
短周期元素ZW的某种微粒的结构示意图如下,下列说法一定不正确的是( )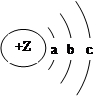
| A.Z=a+b+c | B.若Z<a+b+c,该微粒一定是原子 |
| C.c≤b=8 | D.若c=b,该微粒可能原子或阴离子 |
下列各组中化合物的性质比较,不正确的是
| A.酸性:HClO4>HBrO4>HIO4 |
| B.稳定性:PH3>H2S>HCl |
| C.碱性:NaOH>Mg(OH)2>Al(OH)3 |
| D.非金属性:F>O>S |