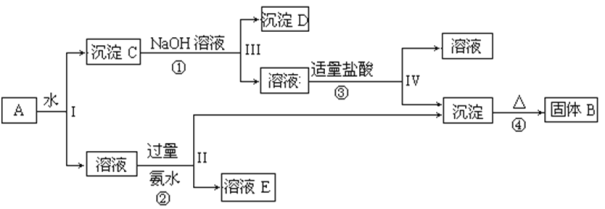
题目内容
【题目】在密闭容器中的一定量混合气体发生反应xM (g)+yN(g)![]() zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
zP(g)。平衡时测得M的浓度为0.80 mol/L,保持温度不变,将容器的容积扩大到原来的两倍,再达平衡时,测得M的浓度降低为0.50 mol/L。下列有关判断正确的是
A.x + y < zB.平衡向正反应方向移动
C.N的转化率降低D.混合气体的密度不变
【答案】C
【解析】
平衡时测得M的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,若平衡不移动,M的浓度变为0.40mol/L,而再达平衡时,测得M的浓度降低为0.50mol/L,由此可知容器容积增大,压强减小,平衡逆向移动了,据此解答。
平衡时测得M的浓度为0.80mol/L,保持温度不变,将容器的容积扩大到原来的两倍,若平衡不移动,M的浓度变为0.40mol/L,而再达平衡时,测得M的浓度降低为0.50mol/L,由此可知容器容积增大,压强减小,平衡逆向移动了,
A. 减小压强,平衡逆向移动,而减压平衡向气体体积增大的方向移动,则x+y > z,A项错误;
B. 由上述分析可知平衡逆向移动,B项错误;
C. 平衡逆向移动,N的转化率降低,C项正确;
D. 根据质量守恒定律知混合气体的质量不变,体积增大,则混合气体的密度减小,D项错误;
答案选C。

练习册系列答案
相关题目