题目内容
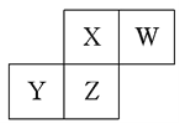
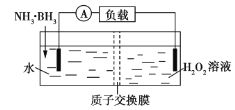
【题目】氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2=NH4BO2+4H2O。已知H2O2足量,下列说法正确的是( )
A.正极的电极反应式为2H++2e-=H2↑
B.电池工作时,H+通过质子交换膜向负极移动
C.电池工作时,正、负极分别放出H2和NH3
D.工作足够长时间后,若左右两极室质量差为1.9g,则电路中转移0.6mol电子
【答案】D
【解析】
以氨硼烷(NH3BH3)电池工作时的总反应为NH3·BH3+3H2O2=NH4BO2+4H2O可知,左侧NH3BH3失电子发生氧化反应为负极,电极反应式为NH3BH3+2H2O-6e-=NH4BO2+6H+,右侧H2O2得到电子发生还原反应为正极,电极反应式为3H2O2+6H++6e-=6H2O,据此分析。
A.右侧H2O2得到电子发生还原反应为正极,电极反应式为3H2O2+6H++6e-=6H2O,A错误;
B.放电时,阳离子向正极移动,所以H+通过质子交换膜向正极移动,B错误;
C.NH3BH3为负极,失电子发生氧化反应,则负极电极反应式为NH3BH3+2H2O-6e-=NH4BO2+6H+,右侧H2O2为正极,得到电子发生还原反应,电极反应式为3H2O2+6H++6e-=6H2O,所以电池工作时,两个电极都不产生气体,C错误;
D.未加入氨硼烷之前,两极室质量相等,通入后,负极电极反应式为NH3BH3+2H2O-6e-=NH4BO2+6H+,正极电极反应式为3H2O2+6H++6e-=6H2O,假设转移电子的物质的量是6mol,则左室质量增加=31g-6g=25g,右室质量增加6g,两极的质量相差19g,理论上转移0.6mol电子,工作一段时间后,若左右两极室质量差为1.9g,则电路中转移0.6 mol电子,D正确;
故合理选项是D。

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案