题目内容
2.CO的应用和治理问题属于当今社会的热点问题.(1)汽车尾气中CO的治理,常用四氧化三钴(Co3O4)纳米棒的作催化剂,低温下与O2反应生成CO2.下列说法中正确的是BD(不定项选择)
A.该反应是分解反应 B.反应前后Co3O4化学性质不改变 C.反应前后碳元素的化合价不变 D.该反应的△H<0
(2)光气(COCl2)是一种重要的化工原料,用于农药、医药、聚酯类材料的生产,工业上通过Cl2(g)+CO(g)?COCl2(g)制备.左图为此反应的反应速率随温度变化的曲线,右图为某次模拟实验研究过程中容器内各物质的浓度随时间变化的曲线.回答下列问题:

①0~6min内,反应的平均速率v(Cl2)=0.15 mol•L-1•min -1;
②若保持温度不变,在第8min加入体系中的三种物质各1mol,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”);
③若将初始投料浓度变为c(Cl2)=0.8mol/L、c(CO)=0.6mol/L、c(COCl2)=0.4 mol/L,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同;
④该反应的平衡常数的表达式为K=$\frac{c(COC{l}_{2})}{c(C{l}_{2})×c(CO)}$,随温度升高,该反应平衡常数变化的趋势为减小(填“增大”、“减小”或“不变”),原因为正反应为放热反应,随温度升高平衡向逆反应方向移动,平衡常数减小;
⑤比较第8min反应温度T(8)与第15min反应温度T(15)的高低:T(8)<T(15)(填“<”、“>”或“=”).
分析 (1)A.反应物为CO、氧气,生成物为二氧化碳;
B.催化剂在反应前后质量不变、化学性质不变;
C.反应中碳元素化合价由+2甲升高为+4价;
D.本质是CO燃烧生成二氧化碳,属于放热反应;
(2)①由图可知,6min时Cl2的平衡浓度为0.3mol/L,浓度变化为1.2mol/L-0.3mol/L=0.9mol/L,根据v=$\frac{△c}{△t}$计算v(Cl2);
②原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,现在第8 min 加入体系中的三种物质各1 mol,则反应物的浓度增大程度大些,平衡正向移动.
③改变初始投料浓度变,保持反应温度不变,则最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同,则为等效平衡,完全转化到左边满足Cl2浓度为1.2mol/L、CO浓度为1.0mol/L;
④平衡常数是生成物平衡浓度化学计量数幂乘积与反应物平衡浓度化学计量数幂乘积的比;由图可知,升温平衡向逆反应方向移动,平衡常数减小;
⑤第8min反应处于平衡状态,在第10分钟时是改变温度使平衡向逆反应方向移动,由④升温平衡向逆反应方向移动,可知正反应为放热反应,升高温度平衡向逆反应方向移动.
解答 解:(1)A.反应方程式为2CO+O2$\frac{\underline{\;Co_{3}O_{4}\;}}{\;}$2CO2,两种物质生成一种物质,为化合反应,故A正确;
B.在反应中,四氧化三钴起到催化剂的作用,反应前后质量和性质都没有发生改变,故B正确;
C.属于氧化还原反应,反应中C元素的化合价发生变化,由+2价升高到+4价,故C错误;
D.本质是CO燃烧生成二氧化碳,属于放热反应,故D正确.
故选:BD;
(2)①由图可知,6min时Cl2的平衡浓度为0.3mol/L,浓度变化为1.2mol/L-0.3mol/L=0.9mol/L,则v(Cl2)=$\frac{0.9mol/L}{6min}$=0.15 mol•L-1•min -1,
故答案为:0.15 mol•L-1•min -1;
②8min时,平衡时c(Cl2)=0.3mol/L、c(CO)=0.1mol/L、c(COCl2)=0.9mol/L,则原平衡时n(Cl2):n(CO):n(COCl2)=3:1:9,现在第8 min 加入体系中的三种物质各1 mol,则反应物的浓度增大程度大些,平衡正向移动,
故答案为:向正反应方向;
③最终达到化学平衡时,Cl2的体积分数与上述第6min时Cl2的体积分数相同,即与开始平衡为等效平衡,完全转化到左边满足Cl2浓度为1.2mol/L、CO浓度为1.0mol/L,则:0.8mol/L+c(COCl2)=1.2mol/L,c(CO)=0.6mol/L+c(COCl2)=1.0mol/L,故c(COCl2)=0.4mol/L,
故答案为:0.4;
④平衡常数K=$\frac{c(COC{l}_{2})}{c(C{l}_{2})×c(CO)}$;由图1可知,升温平衡向逆反应方向移动,正反应为放热反应,所以温度高,平衡常数减小,
故答案为:$\frac{c(COC{l}_{2})}{c(C{l}_{2})×c(CO)}$;减小;正反应为放热反应,随温度升高平衡向逆反应方向移动,平衡常数减小;
⑤根据图象,第8min反应处于平衡状态,在第10分钟时是改变温度使平衡向逆反应方向移动,由④升温平衡向逆反应方向移动,可知正反应为放热反应,升高温度平衡向逆反应方向移动,故T(8)<T(15),
故答案为:<.
点评 本题考查化学平衡计算、化学平衡影响因素、化学平衡常数、反应速率计算等,侧重考查学生对图象与数据的分析及计算能力,难度中等.

 名校课堂系列答案
名校课堂系列答案| 药品柜编号 | ① | ② | ③ | ④ | … |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸钠 | … |
| A. | ③和① | B. | ④和① | C. | ①和② | D. | ③和④ |
| A. | 标准状况下,2.24LCl2溶于水,转移的电子数目为0.2NA | |
| B. | 标准状况下 11.2 L NO与11.2L O2混合,充分反应后所含分子数为0.75NA | |
| C. | 标准状况下,22.4 LCO和NO的混合气体中所含的氧原子总数为NA | |
| D. | 将含有1molFeCl3的浓溶液完全水解可得到Fe(OH)3胶粒的数目为NA |
| 实验 | 温度/℃ | 起始时R的物质的量/mol | 平衡时气体总物质的量/mol |
| ① | 300 | 2.00 | 2.80 |
| ② | 400 | 2.00 | 3.00 |
| ③ | 400 | 4.00 | a |
| A. | 上述反应中,△H<0 | |
| B. | 实验②中,该反应的平衡常数K=0.5 | |
| C. | 实验①经4 min达到平衡,0~4 min内υ(X)=0.2mol•L-1•min-1 | |
| D. | 实验③中a=6.00 |
 在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:
在一定体积的密闭容器中,进行如下化学反应:CO(g)+H2O(g)?CO2(g)+H2(g),其化学平衡常数K和温度t的关系如下表:| t℃ | 700 | 800 | 830 | 1000 |
| K | 2.6 | 1.7 | 1.0 | 0.9 |
(1)该反应的化学平衡常数表达式K=$\frac{c(C{O}_{2})×c({H}_{2})}{c(CO)×c({H}_{2}O)}$.
(2)该反应为放热反应(填“吸热”或“放热”).
(3)增加H2O(g)的浓度,CO的转化率将增大(填“增大”、“减小”或“不变”).
(4)830℃时,向该容器中加入2molCO2与2molH2,平衡时CO2的体积分数是25%.
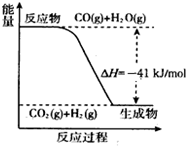
(5)已知工业制氢气的反应为CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中能量变化如图所示.又已知2H2(g)+O2(g)═2H2O(g)△H=-484kJ/mol. 结合图象写出CO完全燃烧生成CO2的热化学方程式:2CO(g)+O2(g)?2CO2(g)△H=-566kJ/mol.
| A. | C4H10 | B. | C2H6O | C. | C3H8O | D. | C2H4O2 |
| A. | Al3+、AlO2-、NO3-、Na+ | B. | NO3-、Fe3+、Mg2+、SO42- | ||
| C. | Na+、Ca2+、Cl-、CO32- | D. | K+、Ba2+、Cl-、NO3- |


